
分析 (1)實驗流程為:粗鹽樣品含有Na2SO4、MgCl2、CaCl2等雜質,加入過量的氯化鋇,可以將硫酸根離子除去,但是會引入鋇離子雜質離子,加入過量氫氧化鈉溶液的目的是除去氯化鎂,加入過量的碳酸鈉溶液的目的除去雜質CaCl2和加入的過量試劑BaCl2,過濾,將得到的沉淀全部濾出,得到的濾液是含有氯化鈉、碳酸鈉、氫氧化鈉等的混合物,加入足量的鹽酸,可以出去碳酸根離子、氫氧根離子等雜質離子,最后即可獲得較為純凈的氯化鈉,據此進行解答;
(2)先放酒精燈,然后根據酒精燈位置固定鐵圈,再在鐵圈上放上蒸發皿,用酒精燈加熱蒸發,當出現大量固體時停止加熱,據此進行排序;
(3)硫酸根離子與鋇離子反應生成硫酸鋇沉淀,用氯化鋇溶液檢驗和除去硫酸根離子;
(4)用碳酸鈉溶液除去過量的鋇離子和雜質鈣離子;
(5)生成的沉淀有氫氧化鎂、碳酸鋇、碳酸鈣、硫酸鋇沉淀;
(6)根據溶解、過濾、蒸發的操作方法判斷玻璃杯的作用.
解答 解:(1)含硫酸鎂和泥沙的粗食鹽提純氯化鈉,溶于水后,加NaOH除去鎂離子,加氯化鋇除去硫酸根離子,再加碳酸鈉除去鋇離子,過濾除去鋇離子,最后加鹽酸,但碳酸鈉一定在氯化鋇之后,則合理的順序為:(5)(4)(2)(1)(3)或(2)(5)(4)(1)(3),
故答案為:A;
(2)蒸發氯化鈉溶液時,先放置酒精燈,再固定鐵圈、放上蒸發皿,然后開始加熱攪拌,當剩余少量液體時停止加熱,所以正確的操作順序為:②①③④⑤,
故答案為:②①③④⑤;
(3)加入過量氯化鋇溶液除去硫酸根離子,檢驗硫酸根離子已除盡,可靜止片刻在上層清液處,滴加一滴氯化鋇溶液,不出現渾濁就說明硫酸根離子已經除盡;
除去硫酸根離子的方法是在溶液中加入過量的氯化鋇溶液;
故答案為:靜置片刻后,取上層清液于試管中,滴加氯化鋇,若出現渾濁或白色沉淀,說明溶液中含有硫酸根離子,反之則沒有;除去硫酸根離子的方法是在溶液中加入過量的氯化鋇溶液;
(4)由于加入的氯化鋇過量,則加入碳酸鈉溶液的目的是除去Ca2+以及加入的過量Ba2+,
故答案為:除去Ca2+以及加入的過量Ba2+;
(5)經過(4)過濾之后得到的沉淀的成分有:Mg(OH)2、BaSO4、CaCO3、BaCO3,
故答案為:Mg(OH)2、BaSO4、CaCO3、BaCO3;
(6)粗鹽制成精鹽的過程中,溶解、過濾、蒸發三個步驟的操作中都要用到玻璃棒,溶解時攪拌可加速溶解;過濾時引流使液體沿著玻璃棒流下;蒸發時提高玻璃杯的攪拌,防止因局部過熱液滴或晶體飛濺,
故答案為:攪拌,加速溶解;引流(或使待濾液體沿玻璃棒流入漏斗,防止外灑);攪拌,防止因局部過熱液滴或晶體飛濺.
點評 本題考查了物質分離與提純方法的綜合應用,題目難度中等,明確加入試劑的先后順序及常見離子的檢驗方法為解答關鍵,注意掌握常見化學實驗基本操作方法,試題培養了學生的分析能力及靈活應用能力.


科目:高中化學 來源: 題型:選擇題
| A. | 增加A的量,平衡正向移動,達到新平衡時K值增大 | |
| B. | 升高溫度,K值增大 | |
| C. | K越大,說明該反應的進行程度越大 | |
| D. | 該反應的K=$\frac{{c}^{m}(A)+cn(B)}{{c}^{p}(C)+{c}^{q}(D)}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③④⑥⑧ | B. | ①④⑥⑧ | C. | ①④⑤⑥⑦ | D. | ②⑤⑧ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
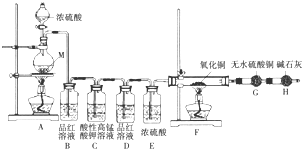
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
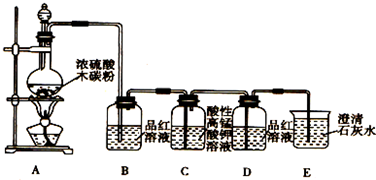
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com