

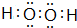 .
.分析 將D溶液滴入沸水中可得到以F為分散質的紅褐色液體,說明F為Fe(OH)3,D含有鐵離子,A和稀硫酸反應生成C、和S反應生成硫化物B,B和濃硫酸反應生成含有鐵離子的D且D中含有硫酸根離子,所以D為Fe2(SO4)3,則A為Fe、B為FeS、C為FeSO4,硫酸亞鐵和雙氧水反應生成硫酸鐵,硫酸鐵和氨水反應生成E和F,硫酸亞鐵和過氧化鈉反應生成F,則E為(NH4)2SO4,H為H2SO4,結合題目分析解答.
解答 解:將D溶液滴入沸水中可得到以F為分散質的紅褐色液體,說明F為Fe(OH)3,D含有鐵離子,A和稀硫酸反應生成C、和S反應生成硫化物B,B和濃硫酸反應生成含有鐵離子的D且D中含有硫酸根離子,所以D為Fe2(SO4)3,則A為Fe、B為FeS、C為FeSO4,硫酸亞鐵和雙氧水反應生成硫酸鐵,硫酸鐵和氨水反應生成E和F,硫酸亞鐵和過氧化鈉反應生成F,則E為(NH4)2SO4,H為H2SO4,
(1)紅褐色液體是氫氧化鐵膠體,分散質粒子直徑大小的范圍是1nm-100nm,
故答案為:1nm-100nm;
(2)A、B、H的化學式分別為Fe、FeS、H2SO4,故答案為:Fe;FeS;H2SO4;
(3)①H2O2分子的電子式: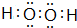 ,
,
故答案為: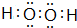 ;
;
②硫酸鐵溶液與氨水氣反應生成氫氧化鐵與硫酸銨,反應離子方程式為Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+,故答案為:Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+;
(4)E中有銨根離子,可取少量E于試管中,用膠頭滴管加入溶液,加熱試管,可觀察到試管口處濕潤的紅色石蕊試紙變藍,說明有銨根離子,
故答案為:取少量E于試管中,用膠頭滴管加入溶液,加熱試管,可觀察到試管口處濕潤的紅色石蕊試紙變藍;
(5)在C(FeSO4)溶液中加入與C等物質的量的Na2O2,恰好使C轉化為F(Fe(OH)3),反應的離子方程式為:4Fe2++4Na2O2+6H2O═4Fe(OH)3+O2↑+8Na+;
故答案為:4Fe2++4Na2O2+6H2O═4Fe(OH)3+O2↑+8Na+.
點評 本題考查無機物推斷,為高頻考點,側重考查學生分析判斷能力,明確Fe及其化合物之間的轉化、離子檢驗方法、氧化還原反應等知識點是解本題關鍵,注意硫酸亞鐵和過氧化鈉的反應,題目難度中等.


 備戰中考寒假系列答案
備戰中考寒假系列答案科目:高中化學 來源: 題型:解答題
| 容器編號 | c(H2O)/mol/L | c(CO)/mol/L | c(H2)/mol/L | V正、V逆比較 |
| Ⅰ | 0.06 | 0.60 | 0.10 | V正=V逆 |
| Ⅱ | 0.06 | 0.50 | 0.40 | ① |
| Ⅲ | 0.12 | 0.40 | 0.80 | V正<V逆 |
| Ⅳ | 0.12 | 0.30 | ② | V正=V逆 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
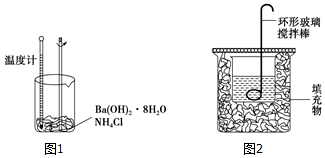
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 22.4LO2中所含氧氣分子計量為1摩爾 | |
| B. | 1mol氧含6.02×1023個O2 | |
| C. | 摩爾是國際科學界建議采用的一種物理量 | |
| D. | 摩爾是物質的量的單位,簡稱摩,符號為mol |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 物質類別 | 酸 | 堿 | 鹽 | 金屬氧化物 | 非金屬氧化物 |
| 化學式 | ①HCl ②H2SO4、H2CO3、H2SO3、H2S | ③NaOH、KOH ④Ba(OH)2 | ⑤Na2SO4 ⑥Na2CO3、Na2SO4、Na2SO3、Na2S | ⑦Na2O | ⑧CO2 ⑨H2O2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com