
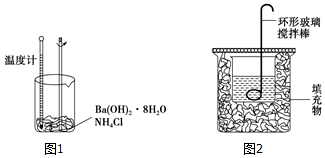
分析 I.(1)發生復分解反應生成氯化鋇、一水合氨、水;
(2)該反應吸收熱量,無元素的化合價變化,為化合物與化合物反應生成新的化合物;
Ⅱ.(1)圖2中缺少溫度計測定溫度;
(2)環形玻璃攪拌棒上下運動攪拌;
(3)稀的酸堿反應生成1mol水的熱量為中和熱;
(4)a.裝置保溫、隔熱效果差,測得的熱量偏小;
b.量取NaOH溶液的體積時仰視讀數,會導致所量的氫氧化鈉體積偏大,放出的熱量偏高;
c.分多次把NaOH溶液倒入盛有硫酸的小燒杯中,熱量散失較多;
d.溫度計測定NaOH溶液起始溫度后直接插入稀H2SO4測溫度,硫酸的起始溫度偏高.
解答 解:Ⅰ.(1)Ba(OH)2•8H2O跟NH4Cl反應的化學方程式為Ba(OH)2•8H2O+2NH4Cl=BaCl2+8H2O+2NH3•H2O,
故答案為:Ba(OH)2•8H2O+2NH4Cl=BaCl2+8H2O+2NH3•H2O;
(2)該反應吸收熱量,為吸熱反應;無元素的化合價變化,屬于非氧化還原反應;為化合物與化合物反應生成新的化合物,屬于復分解反應,
故答案為:吸熱;非氧化還原;復分解反應;
Ⅱ.(1)圖中尚缺少的一種儀器是溫度計,故答案為:溫度計;
(2)環形玻璃攪拌棒上下運動攪拌,故答案為:a;
(3)反應的熱化學方程式為為HCl (aq)+NaOH(aq)=NaCl(aq)+H2O(l)△H=-57.3KJ/mol,
故答案為:HCl (aq)+NaOH(aq)=NaCl(aq)+H2O(l)△H=-57.3KJ/mol;
(4)a.裝置保溫、隔熱效果差,測得的熱量偏小,中和熱的數值偏小,故a正確;
b.量取NaOH溶液的體積時仰視讀數,會導致所量的氫氧化鈉體積偏大,放出的熱量偏高,中和熱的數值偏大,故b錯誤;
c.分多次把NaOH 溶液倒人盛有硫酸的小燒杯中,熱量散失較多,測得溫度偏低,中和熱的數值偏小,故c正確;
d.溫度計測定NaOH溶液起始溫度后直接插入稀H2SO4測溫度,硫酸的起始溫度偏高,溫度差偏小,測得的熱量偏小,中和熱的數值偏小,故d正確.
故答案為:acd.
點評 本題考查中和熱測定實驗,為高頻考點,把握測定原理、實驗操作、實驗技能為解答的關鍵,側重分析與實驗能力的考查,注意中和熱的數值及誤差分析,題目難度不大.


 小學教材全測系列答案
小學教材全測系列答案 小學數學口算題卡脫口而出系列答案
小學數學口算題卡脫口而出系列答案 優秀生應用題卡口算天天練系列答案
優秀生應用題卡口算天天練系列答案 浙江之星課時優化作業系列答案
浙江之星課時優化作業系列答案科目:高中化學 來源: 題型:解答題
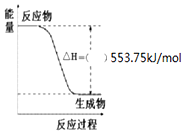 按要求寫出298K、101kPa時下列反應的熱化學方程式:
按要求寫出298K、101kPa時下列反應的熱化學方程式:查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | BrCl的化學性質和Cl2相似,Cl2與水反應是氧化還原反應,BrCl+H2O=HCl+HBrO也是氧化還原反應 | |
| B. | 弱堿性條件下,甲酸乙酯能與氫氧化銅反應,乙酸乙酯也能與氫氧化銅反應 | |
| C. | 苯不能使酸性高錳酸鉀褪色,甲苯也不能使酸性高錳酸鉀褪色 | |
| D. | CO2與SiO2均為酸性氧化物,CO2能與NaOH溶液反應,SiO2也能與NaOH溶液反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題

 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
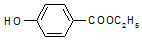 ,生產過程如圖:
,生產過程如圖: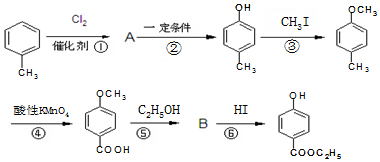
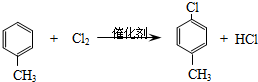 .
. ,-X、-Y為取代基)是對羥基苯甲酸乙酯的同分異構體且能發生銀鏡反應,則-X的結構簡式可能是-OH、-CH2OH 或-OCH3.
,-X、-Y為取代基)是對羥基苯甲酸乙酯的同分異構體且能發生銀鏡反應,則-X的結構簡式可能是-OH、-CH2OH 或-OCH3.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO2 | B. | NO2 | C. | PM2.5 | D. | CO2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com