
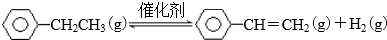
| 化學鍵 | C-H | C-C | C=C | H-H |
| 鍵能/kJ•molˉ1 | 412 | 348 | 612 | 436 |
分析 (1)反應熱=反應物總鍵能-生成物總能鍵能,由有機物的結構可知,應是-CH2CH3中總鍵能與-CH=CH2、H2總鍵能之差;
(2)參加反應的乙苯為nα mol,則:
 ?
? +H2
+H2
開始(mol):n 0 0
轉化(mol):nα nα nα
平衡(mol):n(1-α) nα nα
維持體系總壓強p恒定,在溫度T時,由PV=nRT可知,混合氣體總濃度不變,設反應后的體積為V′,則$\frac{n(1-α)+nα+nα}{V′}$=$\frac{n}{V}$,故V′=(1+α)V,再根據平衡常數表達式K=$\frac{c(苯乙烯)×c({H}_{2})}{c(乙苯)}$計算解答;
(3)①保持壓強不變,加入水蒸氣,容器體積應增大,等效為降低壓強,平衡向氣體體積增大的方向移動;
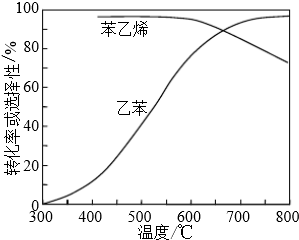
②600℃時乙苯的轉化率與苯乙烯的選擇性均較高;結合溫度對乙苯轉化率、苯乙烯選擇性、溫度對反應速率與催化劑的影響及消耗能量等,分析控制反應溫度為600℃的理由;
(4)①CO2與H2反應,導致氫氣濃度減低,有利于乙苯脫氫反應的化學平衡右移;
②由題目信息可知,在保持常壓和原料氣比例不變,與摻水蒸汽工藝相比,在相同的生產效率下,可降低操作溫度,消耗的能量減少;
③由于會發生反應CO2+C═2CO,有利于減少積炭;
④CO2代替水蒸氣,有利用CO2資源利用.
解答 解:(1)反應熱=反應物總鍵能-生成物總能鍵能,由有機物的結構可知,應是-CH2CH3中總鍵能與-CH=CH2、H2總鍵能之差,故△H=(5×412+348-3×412-612-436)kJ•mol-1=+124kJ•mol-1,
故答案為:+124;
(2)物質的量為n、體積為V的乙苯蒸氣發生催化脫氫反應
參加反應的乙苯為nα mol,則:
 ?
? +H2
+H2
開始(mol):n 0 0
轉化(mol):nα nα nα
平衡(mol):n(1-α) nα nα
維持體系總壓強p恒定,在溫度T時,由PV=nRT可知,混合氣體總濃度不變,設反應后的體積為V′,則$\frac{n(1-α)+nα+nα}{V′}$=$\frac{n}{V}$,故V′=(1+α)V,則平衡常數K=$\frac{c(苯乙烯)×c({H}_{2})}{c(乙苯)}$=$\frac{\frac{nα}{(1+α)V}×\frac{nα}{(1+α)V}}{\frac{n(1-α)}{(1+α)V}}$=$\frac{n{α}^{2}}{(1-{α}^{2})V}$,
故答案為:$\frac{n{α}^{2}}{(1-{α}^{2})V}$;
(3)①正反應為氣體分子數增大的反應,保持壓強不變,加入水蒸氣,容器體積應增大,等效為降低壓強,平衡向正反應方向移動,提高乙苯的平衡轉化率,
故答案為:正反應為氣體分子數增大的反應,保持壓強不變,加入水蒸氣,容器體積應增大,等效為降低壓強,平衡向正反應方向移動;
②600℃時乙苯的轉化率與苯乙烯的選擇性均較高,溫度過低,反應速率較慢,轉化率較低,溫度過高,選擇性下降,高溫下可能失催化劑失去活性,且消耗能量較大,故選擇600℃左右,
故答案為:600℃時乙苯的轉化率與苯乙烯的選擇性均較高,溫度過低,反應速率較慢,轉化率較低,溫度過高,選擇性下降,高溫下可能失催化劑失去活性,且消耗能量較大;
(4)①CO2與H2反應,導致氫氣濃度減低,有利于乙苯脫氫反應的化學平衡右移,故正確;
②由題目信息可知,在保持常壓和原料氣比例不變,與摻水蒸汽工藝相比,在相同的生產效率下,可降低操作溫度,消耗的能量減少,故正確;
③由于會發生反應CO2+C═2CO,有利于減少積炭,故正確;
④CO2代替水蒸氣,有利用CO2資源利用,故正確,
故選:①②③④.
點評 本題考查反應熱計算、化學平衡常數計算、反應速率及平衡移動的影響因素、對條件控制的分析評價等,(1)中認為苯環存在單雙鍵交替形式不影響計算結構,(2)中平衡常數計算為易錯點、難點,注意溫度、壓強不變,容器的體積發生變化,學生容易認為容器的體積不變,題目難度較大.


科目:高中化學 來源: 題型:解答題
| 族 周期 | IA | 0 | |||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ① | Be | ② | ③ | Ne | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | |||||
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 550℃時,若充入惰性氣體,v正,v退均減小,平衡不移動 | |
| B. | 650℃時,反應達平衡后CO2的轉化率為25.0% | |
| C. | T℃時,若充入等體積的CO2和CO,平衡向逆反應方向移動 | |
| D. | 925℃時,用平衡分壓代替平衡濃度表示的化學平衡常數Kp=24.0P總 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NO2 | B. | SO2 | C. | SO3 | D. | CO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 (或
(或
 );
);查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 物質 選項 | X | Y |
| A | Na2CO3 | NaHCO3 |
| B | Al(OH)3 | Al2O3 |
| C | FeCl3 | FeCl2 |
| D | CuSO4 | Cu(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com