
分析 8NH3+3Cl2═6NH4Cl+N2中,N元素的化合價由-3價升高為0,Cl元素的化合價由0降低為-1價,以此來解答.
解答 解:(1)Cl元素的化合價降低,則Cl2為氧化劑,被還原,還原產物為NH4Cl,N元素的化合價升高,失去電子被氧化,還原劑為NH3,
故答案為:Cl2;N;
(2)還原劑為NH3,還原產物為NH4Cl,還原劑與還原產物的物質的量之比是2:6=1:3,故答案為:1:3;
(3)由方程式可知,8molNH3參加反應時,其中2mol作還原劑被氧化,則當有34g、即2molNH3參加反應時,被氧化的物質的質量為2mol×$\frac{1}{4}$×17g/mol=8.5g,生成的還原產物的質量為2mol×$\frac{3}{4}$×53.5g/mol=80.25g,故答案為:8.5;80.25.
點評 本題考查氧化還原反應及計算,為高頻考點,把握反應中元素的化合價變化為解答的關鍵,側重氧化還原反應基本概念及計算的考查,注意8molNH3中只有2mol為還原劑,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 1 mol/L Na2CO3溶液中的Na+ 數目為2NA | |
| B. | 7.8 g Na2O2所含離子總數為0.4 NA | |
| C. | 1 mol Na與足量O2反應生成Na2O或Na2O2均失去NA電子 | |
| D. | 34 g OH-中含質子數20NA |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ba(OH)2與稀H2SO4反應:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | 氫氧化鎂與鹽酸的反應:OH-+H +═H2O | |
| C. | Cl2與NaOH 溶液反應:Cl2+2OH-═Cl-+ClO- | |
| D. | 碳酸鈣溶于稀鹽酸中CaCO3+2H═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | OH- | B. | SO${\;}_{4}^{2-}$ | C. | Ba2+ | D. | Cu2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
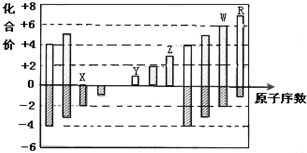
| A. | 原子半徑:Z>Y>X | |
| B. | 氣態氫化物的穩定性:R>W | |
| C. | 最高價氧化物的水化物的堿性:Y<Z | |
| D. | Y和Z兩者最高價氧化物對應的水化物能相互反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C8H10 | B. | CH4 | C. | CH3CH2OH | D. | C5H10 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com