
【題目】設NA表示阿伏加德羅常數的值。下列說法正確的是( )
A.14g聚丙烯中含C-H鍵總數目為2NA
B.常溫下,pH=13的NaOH溶液中含有的OH-數目為0.1NA
C.100mL12mol·L-1濃硝酸與過量Cu反應轉移電子的數目為0.6NA
D.電解精煉銅時,若陽極質量減少64g,則陰極得到電子的數目為2NA
【答案】A
【解析】
A. 聚丙烯的最簡式為CH2,14g聚丙烯中含H:![]() ,所有H均與C以單鍵相連,所以C-H鍵總數目為2NA,A選項正確;
,所有H均與C以單鍵相連,所以C-H鍵總數目為2NA,A選項正確;
B. 沒有提供體積,無法計算OH-數目,B選項錯誤;
C. 100mL12mol·L-1濃硝酸中HNO3的物質的量為:100×10-3L×12mol·L-1=1.2mol。與過量Cu反應,先:Cu + 4HNO3(濃) = Cu(NO3)2 + 2NO2↑ + 2H2O,參加反應的HNO3數目和轉移電子的數目的關系為2:1;硝酸變稀后:3Cu + 8HNO3(稀) = 3Cu(NO3)2 + 2NO↑ + 4H2O,參加反應的HNO3數目和轉移電子的數目的關系為4:3。所以,轉移電子的數目為0.6NA和0.9NA之間,C選項錯誤;
D. 電解精煉銅時,陽極溶解的除了Cu還有比Cu活潑的金屬,所以若陽極質量減少64g,則陰極得到電子的數目不為2NA,選項D錯誤;
答案選A。


科目:高中化學 來源: 題型:
【題目】某校化學課外興趣小組為了探究影響化學反應速率的因素,做了以下實驗。
(1)用三支試管各取5.0 mL、0.01 mol·L-1的酸性KMnO4溶液,再分別滴入0.1 mol·L-1 H2C2O4溶液,實驗報告如下。

①實驗1、3研究的是_________對反應速率的影響。
②表中V=_________mL。
(2)小組同學在進行(1)中各組實驗時,均發現該反應開始時很慢,一段時間后速率會突然加快。對此該小組的同學展開討論:
①甲同學認為KMnO4與H2C2O4的反應放熱,溫度升高,速率加快。
②乙同學認為隨著反應的進行,因_________,故速率加快。
(3)為比較Fe3+、Cu2+對H2O2分解的催化效果,該小組的同學又分別設計了如圖甲、乙所示的實驗。回答相關問題:

①裝置乙中儀器A的名稱為_________。
②定性如圖甲可通過觀察反應產生氣泡的快慢,定性比較得出結論。有同學提出將CuSO4溶液改為CuCl2溶液更合理,其理由是____________________________________。
③定量如圖乙所示,實驗時以收集到40 mL氣體為準,忽略其他可能影響實驗的因素,實驗中需要測量的數據是_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是閃鋅礦(主要成分是ZnS,含有少量FeS)制備ZnSO4·7H2O的一種工藝流程:閃鋅礦粉→溶浸→除鐵→結晶→ZnSO47H2O。已知:相關金屬離子濃度為0.1mol/L時形成氫氧化物沉淀的pH范圍如表:
金屬離子 | Fe3+ | Fe2+ | Zn2+ |
開始沉淀的pH | 1.5 | 6.3 | 6.2 |
沉淀完全的pH | 2.8 | 8.3 | 8.2 |
(1)閃鋅礦在溶浸之前會將其粉碎,其目的是_____________。
(2)溶浸過程使用過量的Fe2(SO4)3溶液和H2SO4浸取礦粉,發生的主要反應是:ZnS+2Fe3+=Zn2++2Fe2++S。
①浸出液中含有的陽離子包括Zn2+、Fe2+、_____________。
②若改用CuSO4溶液浸取,發生復分解反應,也能達到浸出鋅的目的,寫出離子方程式_____________。
(3)工業除鐵過程需要控制沉淀速率,因此分為還原和氧化兩步先后進行,如圖。還原過程將部分Fe3+轉化為Fe2+,得到pH小于1.5的溶液。氧化過程向溶液中先加入氧化物a,再通入O2。下列說法正確的是_____________(填序號)。
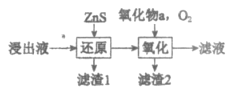
A. 氧化物a可以是ZnO
B. 濾渣2的主要成分是Fe(OH)2
C. 加入ZnS的量和通入O2的速率都可以控制溶液中的c(Fe3+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某混合物漿液含Al(OH)3、MnO2和少量Na2Cr2O4。考慮到膠體的吸附作用使Na2Cr2O4不易完全被水浸出,某研究小組利用設計的電解分離裝置(如圖1),使漿液分離成固體混合物和含鉻元素溶液,并回收利用。
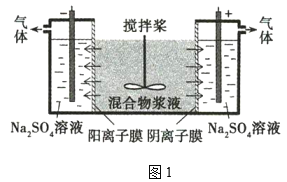
固體混合物的分離和利用的流程圖如圖2所示(流程圖中的部分分離操作和反應條件未標明):
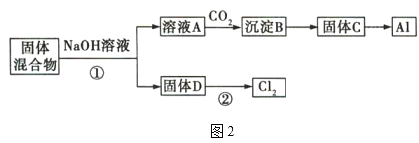
(1)反應①所加試劑NaOH的電子式為___,B→C的反應條件為___,C→Al的制備方法稱為___。
(2)該小組探究反應②發生的條件。D與濃鹽酸混合,不加熱,無變化;加熱有Cl2生成,當反應停止后,固體有剩余,此時滴加硫酸,又產生Cl2。由此判斷影響該反應有效進行的因素有___(填序號)。
a.溫度 b.Cl-的濃度 c.溶液的酸度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】N2O、NO和NO2等氮氧化物是空氣污染物,含有氮氧化物的尾氣需處理后才能排放。
(1)N2O的處理。N2O是硝酸生產中氨催化氧化的副產物,用特種催化劑能使N2O分解。NH3與O2在加熱和催化劑作用下生成N2O的化學方程式為________。
(2)NO和NO2的處理。已除去N2O的硝酸尾氣可用NaOH溶液吸收,主要反應為
NO+NO2+2OH![]() 2
2![]() +H2O
+H2O
2NO2+2OH![]()
![]() +
+![]() +H2O
+H2O
①下列措施能提高尾氣中NO和NO2去除率的有________(填字母)。
A.加快通入尾氣的速率
B.采用氣、液逆流的方式吸收尾氣
C.吸收尾氣過程中定期補加適量NaOH溶液
②吸收后的溶液經濃縮、結晶、過濾,得到NaNO2晶體,該晶體中的主要雜質是________(填化學式);吸收后排放的尾氣中含量較高的氮氧化物是________(填化學式)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾氣,可提高尾氣中NO的去除率。其他條件相同,NO轉化為![]() 的轉化率隨NaClO溶液初始pH(用稀鹽酸調節)的變化如圖所示。
的轉化率隨NaClO溶液初始pH(用稀鹽酸調節)的變化如圖所示。
①在酸性NaClO溶液中,HClO氧化NO生成Cl和![]() ,其離子方程式為________。
,其離子方程式為________。
②NaClO溶液的初始pH越小,NO轉化率越高。其原因是________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在25℃時,將兩個銅電極插入一定量的硫酸鈉飽和溶液中進行電解,通電一段時間后,陰極逸出amol氣體,同時有wgNa2SO4·10H2O晶體析出,若溫度不變,剩余溶液的溶質質量分數是( )
A.![]() %B.
%B.![]() %C.
%C.![]() %D.
%D.![]() %
%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(題文)化合物N具有鎮痛、消炎等藥理作用,其合成路線如下:

(1)A的系統命名為____________,E中官能團的名稱為____________。
(2)A→B的反應類型為____________,從反應所得液態有機混合物中提純B的常用方法為____________。
(3)C→D的化學方程式為________________________。
(4)C的同分異構體W(不考慮手性異構)可發生銀鏡反應:且1 mol W最多與2 mol NaOH發生反應,產物之一可被氧化成二元醛。滿足上述條件的W有____________種,若W的核磁共振氫譜具有四組峰,則其結構簡式為____________。
(5)F與G的關系為(填序號)____________。
a.碳鏈異構 b.官能團異構 c.順反異構 d.位置異構
(6)M的結構簡式為____________。
(7)參照上述合成路線,以![]() 為原料,采用如下方法制備醫藥中間體
為原料,采用如下方法制備醫藥中間體![]() 。
。

該路線中試劑與條件1為____________,X的結構簡式為____________;
試劑與條件2為____________,Y的結構簡式為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有研究人員在體外實驗中發現藥物瑞德西韋對新冠病毒有明顯抑制作用。E是合成瑞德西韋的中間體,其合成路線如下:
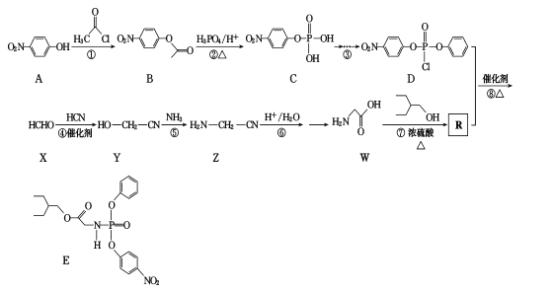
回答下列問題:
(1)W的化學名稱為____;反應①的反應類型為____
(2)A中含氧官能團的名稱為____。
(3)寫出反應⑦的化學方程式_____
(4)滿足下列條件的B的同分異構體有____種(不包括立體異構)。
①苯的二取代物且苯環上含有硝基;②可以發生水解反應。
上述同分異構體中核磁共振氫譜為3:2:2的結構簡式為____________
(5)有機物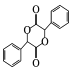 中手性碳(已知與4個不同的原子或原子團相連的碳原子稱為手性碳)有 ___個。結合題給信息和已學知識,設計由苯甲醇為原料制備
中手性碳(已知與4個不同的原子或原子團相連的碳原子稱為手性碳)有 ___個。結合題給信息和已學知識,設計由苯甲醇為原料制備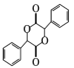 的合成路線_______ (無機試劑任選)。
的合成路線_______ (無機試劑任選)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E為元素周期表中前四周期元素,原子序數依次增大,A元素原子核外有3個未成對電子,B元素原子核外電子占用3個能級,其中最高能級上的電子數是其所在能層數的2倍,D元素與B元素同族,C元素與A元素同族,E元素原子的價電子數是其余電子數的一半。
(1)A、C、D的第一電離能由大到小的順序為___________________(用元素符號表示),E2+的基態電子排布式為__________________________________。
(2)B和D的氫化物中,B的氫化物沸點較高的原因是____________________________。
(3)C形成的最高價氧化物的結構如圖所示,該結構中C-B鍵的鍵長有兩類,鍵長較短的鍵為__________(填“a”或“b”)。
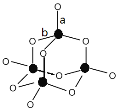
(4)E可與CO形成羰基配合物E2(CO)8,是有機合成的重要催化劑,不溶于水,溶于乙醇、乙醚、苯,熔點50~51℃,45℃(1.33kPa)時升華。
① E2(CO)8為_________晶體。(填晶體類型)
② E2(CO)8晶體中存在的作用力有______________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com