
| A. | 鍍鋅鐵板是利用了犧牲陽極的陰極保護法來達到防止腐蝕的目的 | |
| B. | 反應Hg(1)+H2SO4(aq)═HgSO4(aq)+H2(g)在常溫下不能自發進行,則△H>0 | |
| C. | 將純水加熱至較高溫度,Kw變大、pH變小、呈酸性 | |
| D. | 對于反應2H2O2═2H2O+O2↑,加入MnO2或升高溫度都能加快O2的生成速率 |
分析 A.鋅比鐵活潑,形成原電池反應時鋅為負極;
B.反應不能自發,應滿足△G=△H-T•△S>0,結合反應的△H和△S進行判斷;
C.純水呈中性;
D.加入催化劑或升高溫度,都可增大反應速率.
解答 解:A.鋅比鐵活潑,形成原電池反應時鋅為負極,鋅被氧化,鐵被保護,為犧牲陽極的陰極保護法,故A正確;
B.反應不能自發,應滿足△G=△H-T•△S>0,即△H>T•△S,而反應的△S>0,故△H>0,故B正確;
C.升高溫度,Kw變大、pH變小,但氫離子和氫氧根離子濃度相等,純水呈中性,故C錯誤;
D.加入催化劑或升高溫度,都可增大活化分子百分數,增大反應速率,故D正確.
故選C.
點評 本題考查較綜合,涉及弱電解質的電離、電解原理等知識點,明確物質的性質及反應原理是解本題關鍵,易錯選項是C,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | U元素的近似相對原子質量為235 | |
| B. | ${\;}_{92}^{235}$U中中子數比質子數多51 | |
| C. | ${\;}_{92}^{235}$U與${\;}_{6}^{12}$C的質量比約為235:12 | |
| D. | ${\;}_{92}^{235}$U 與${\;}_{92}^{238}$U屬于同一種元素 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
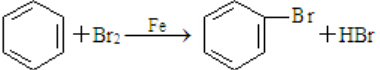 ;
; .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 濃氨水中滴加FeCl3飽和溶液可制得Fe(OH)3膠體 | |
| B. | 一定溫度下,pH相同的①CH3COONa、②NaHCO3、③NaClO三種溶液的c(Na+):①>②>③ | |
| C. | CH3COONa溶液中滴加少量濃鹽酸后c(CH3COO-)增大 | |
| D. | 25℃時Cu(OH)2在水中的溶解度大于其在Cu(NO3)2溶液中的溶解度 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH<7的雨水就是酸雨 | |
| B. | 綠色化學的核心就是利用化學原理從源頭上減少和消除工業生產對環境的影響 | |
| C. | 含氮、磷的大量污水任意排放是導致水華的主要原因 | |
| D. | 垃圾是放錯地方的資源,應該分類回收利用 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 葡萄糖能發生氧化反應和水解反應 | |
| B. | 淀粉在稀酸催化下,最終水解為葡萄糖 | |
| C. | 蛋白質在酶催化下可水解成氨基酸 | |
| D. | 油脂在堿性條件下的水解反應又叫皂化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 容器內的密度不再變化 | |
| B. | C的生成速率與A的分解速率之比為2:1 | |
| C. | 混合物的平均摩爾質量不再變化 | |
| D. | 容器內的溫度不再發生變化 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com