
分析 2分鐘后測得SO2的濃度為0.25mol•L-1,則△c(SO2)=(0.5-0.25)mol/L=0.25mol/L,根據v=$\frac{△c}{△t}$計算二氧化硫的平均反應速率,再根據同一可逆反應同一時間段內各物質的反應速率之比等于其計量數之比計算氧氣反應速率,從而確定v(SO2):v(SO3):v(O2)的值.
解答 解:2分鐘后測得SO2的濃度為0.25mol•L-1,則△c(SO2)=(0.5-0.25)mol/L=0.25mol/L,v(SO2)=$\frac{△c}{△t}$=$\frac{0.25}{2}$mol•L-1•min-1=0.125mol•L-1•min-1,同一可逆反應同一時間段內各物質的反應速率之比等于其計量數之比得氧氣反應速率=$\frac{1}{2}$v(SO2)=$\frac{1}{2}$×0.125mol•L-1•min-1=0.0625 mol•L-1•min-1,同一可逆反應同一時間段內各物質的反應速率之比等于其計量數之比,所以v(SO2):v(SO3):v(O2)=2:2:1,
故答案為:0.0625 mol•L-1•min-1;2:2:1.
點評 本題考查化學反應速率的有關計算,明確反應速率之比與計量數之比關系是解本題關鍵,側重考查學生計算能力,題目難度不大.


科目:高中化學 來源: 題型:解答題
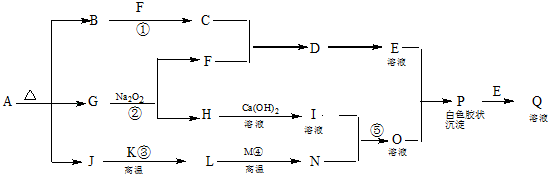
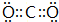 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:解答題

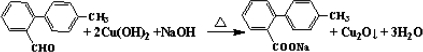 .
. 與
與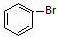 也可以發生類似反應①的反應,有機產物的結構簡式為:
也可以發生類似反應①的反應,有機產物的結構簡式為: .
.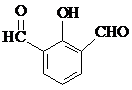 、
、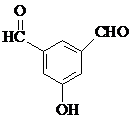 、
、
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2KClO3(s)═2KCl(s)+3O2(g);△H=-78.03kJ•mol-1:△S=494.4 J•mol-1•K-1 | |
| B. | CO(g)═C(s,石墨)+$\frac{1}{2}$O2(g);△H=110.5kJ•mol-1,△S=-89.4 J•mol-1•K-1 | |
| C. | 4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)△H=-444.3kJ•mol-1,△S=-280.1 J•mol-1•K-1 | |
| D. | NH4HCO3(s)+CH3COOH(aq)═CO2(g)+CH3COONH4(aq)+H2O(l);△H=37.30kJ•mol-1,△S=184.0 J•mol-1•K-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鍍鋅鐵板是利用了犧牲陽極的陰極保護法來達到防止腐蝕的目的 | |
| B. | 反應Hg(1)+H2SO4(aq)═HgSO4(aq)+H2(g)在常溫下不能自發進行,則△H>0 | |
| C. | 將純水加熱至較高溫度,Kw變大、pH變小、呈酸性 | |
| D. | 對于反應2H2O2═2H2O+O2↑,加入MnO2或升高溫度都能加快O2的生成速率 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 堿金屬單質的密度隨著原子序數的增大而增大 | |
| B. | 堿金屬單質都是銀白色金屬 | |
| C. | 在周期表中金屬與非金屬的分界處,可以找到半導體材料 | |
| D. | 所有氣體單質都含有非極性鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
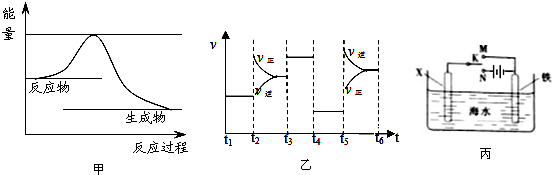
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 氣體 | N2 | O2 | Ar | CO2 |
| 沸點 | -196℃ | -183℃ | -186℃ | -78℃ |
| A. | O2 | B. | N2 | C. | Ar | D. | CO2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com