
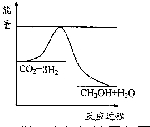
 以煤為原料,經過化學加工使煤轉化為氣體、液體、固體燃料以及各種化工產品的工業叫煤化工.
以煤為原料,經過化學加工使煤轉化為氣體、液體、固體燃料以及各種化工產品的工業叫煤化工.| 起始 濃度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
分析 (1)①在高溫下能自發進行,根據△G=△H-T△S<0判斷;
②結合平衡的特征“等、定”及衍生的物理量判斷,始終不變的量不能判定平衡狀態;
③K是生成物的濃度冪與反應物濃度冪之積的比;
(2)A.丙中濃度最大,甲中濃度最小,濃度越大,反應速率越大;
B. 以甲計算:
H2O(g)+CO(g)?H2(g)+CO2(g)
起始:0 0 0.010 0.010
轉化:x x x x
平衡:x x 0.01-x 0.01-x
則$\frac{(0.01-x)^{2}}{{x}^{2}}$=$\frac{4}{9}$,
x=0.006,結合等效平衡狀態計算;
C.由B計算可知,平衡時,丙中的c(CO2)是甲中的2倍;
D.乙與甲相比較,相當于在甲的基礎上通入H2,則平衡向逆反應方向移動;
(3)A.該反應為放熱反應,升高溫度,平衡逆向移動;
B.充入He(g),使體系壓強增大,但各組分的濃度不變;
C.將H2O(g)從體系中分離出來,生成物濃度減小;
D.再充入1mol CO2 和3mol H2,兩邊的氣體計量數相等,所以平衡時各組分的物質的量是原來的2倍.
解答 解:(1)①在高溫下能自發進行,根據△G=△H-T△S<0,而該反應中△H>0,所以△S>0,故答案為:△S>0;
②A.在一個容積可變的密閉容器,容器中的壓強始終不變,故A錯誤;
B.1mol H-H 鍵斷裂等效于生成2mol H-O 鍵同時斷裂2mol H-O 鍵,正逆反應速率相等,故B正確;
C.V (CO)=V (H2)只要反應發生就符合V (CO)=V (H2),故C錯誤;
D.密閉容器的容積不再改變,說明氣體的物質的量不變,達平衡狀態,故D正確;
E.消耗1mol 水的同時生成1mol H2,都反應的是正反應方向,故E錯誤;
F.容器的密度不變,說明氣體的摩爾質量不變,反應達平衡狀態,故F正確;
故答案為:BDF;
③平衡常數是生成物的濃度冪與反應物濃度冪之積的比,平衡常數的表達式K=$\frac{c(CO)c({H}_{2})}{c({H}_{2}O)}$,故答案為:$\frac{c(CO)c({H}_{2})}{c({H}_{2}O)}$;
(2)A.丙中濃度最大,甲中濃度最小,濃度越大,反應速率越大,則反應開始時,丙中的反應速率最快,甲中的反應最慢,故A正確;
B. 以甲計算:
H2O(g)+CO(g)?H2(g)+CO2(g)
起始:0 0 0.010 0.010
轉化:x x x x
平衡:x x 0.01-x 0.01-x
則$\frac{(0.01-x)^{2}}{{x}^{2}}$=$\frac{4}{9}$,
x=0.006,則平衡時甲中的H2的轉化率均是$\frac{0.006}{0.01}$×100%=60%,由于甲和丙的氣體的比值相同,為等效平衡狀態,則丙中H2的轉化率也為60%,故B錯誤;
C.由B計算可知,平衡時,丙中的c(CO2)是甲中的2倍,應為2×(0.01-0.006)mol/L=0.008mol/L,故C正確;
D.乙與甲相比較,相當于在甲的基礎上通入H2,則平衡向逆反應方向移動,平衡時,乙中的CO2的轉化率大于60%,故D正確.
故答案為:B;
(3)A.升高溫度,平衡逆向移動,能使c(CH3OH)減小,故A正確;
B.充入He(g),使體系壓強增大,但各組分的濃度不變,平衡不移動,故B錯誤;
C.將H2O(g)從體系中分離出來,平衡正向移動,故C錯誤;
D.再充入1mol CO2 和3mol H2,兩邊的氣體計量數相等,所以平衡時各組分的物質的量是原來的2倍,所以濃度不變,故D錯誤;
故答案為:A.
點評 本題考查化學平衡的計算,為高頻考點,把握K的意義、化學平衡移動為解答的關鍵,側重分析與應用能力的考查,注意平衡常數表達式中不能出現固體,題目難度不大.


科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
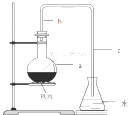 中學實驗室用如圖所示裝置制取少量溴苯.請填寫下列空白.
中學實驗室用如圖所示裝置制取少量溴苯.請填寫下列空白.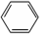 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$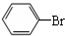 +HBr.
+HBr.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 某溫度時,反應X(g)=4Y(g)+Z(g)△H=-QkJ/mol,在2L的恒容密閉容器中進行,X的濃度隨時間變化如圖所示.下列說法不正確的是( )
某溫度時,反應X(g)=4Y(g)+Z(g)△H=-QkJ/mol,在2L的恒容密閉容器中進行,X的濃度隨時間變化如圖所示.下列說法不正確的是( )| A. | 2min內,X的平均反應速率為0.25mol/(L•min) | |
| B. | 第5min時,該反應達到平衡狀態 | |
| C. | 第5min后,Y的生成速率與X的消耗速率相等且保持不變 | |
| D. | 5min內,反應放出的熱量為1.6QkJ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | MgO和Al2O3在工業上用于制作耐高溫材料,也可用于電解法冶煉Mg、Al | |
| B. | 水泥冶金廠常用高壓電除去工廠煙塵,利用了膠體的性質 | |
| C. | 醫療上用的“鋇餐”其成分是碳酸鋇,漂白粉的成分為次氯酸鈣 | |
| D. | “海水淡化”可以解決“淡水供應危機”,向海水中加入凈水劑明礬可以使海水淡化 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
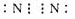 .
.| B-A | B-D | B=D | A-A | A-D |
| 413.4 | 351 | 745 | 436 | 462.8 |
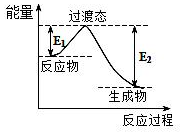
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{83}^{209}$Bi 和${\;}_{83}^{210}$Bi都含有83個中子 | |
| B. | 同位素:H2、D2、T2 | |
| C. | H2O和NH3分子中具有相同的質子數和電子數 | |
| D. | 稀有氣體的原子最外層都達到8電子穩定結構,故都不能與別的物質發生反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com