
| A. | 某些金屬氧化物灼燒時有特殊的顏色,因此可用于制造煙花 | |
| B. | 明礬可用作凈水劑 | |
| C. | 常溫下,將鋁片放入濃硫酸中,無明顯現象,說明鋁不與冷的濃硫酸反應 | |
| D. | 次氯酸鈉溶液可用于環境的消毒殺菌 |
分析 A、金屬元素灼燒發生焰色反應;
B、明礬溶于水電離出的鋁離子,在水溶液中能水解出氫氧化鋁膠體;
C、常溫下,鋁在濃硫酸中會鈍化;
D、次氯酸鈉有強氧化性.
解答 解:A、金屬元素灼燒發生焰色反應,則某些金屬氧化物灼燒時有特殊的顏色,因此可用于制造煙花,故A正確;
B、明礬溶于水電離出的鋁離子,在水溶液中能水解出氫氧化鋁膠體,有吸附性,能吸附水中的雜質而起到凈水的作用,故B正確;
C、常溫下,由于濃硫酸的氧化性很強,能將金屬鋁的表面氧化為一層致密的氧化物薄膜,從而保護內部的鋁不能和濃硫酸繼續反應,即鋁在濃硫酸中會鈍化,故鈍化為反應程度很小的氧化還原反應,故C錯誤;
D、次氯酸鈉有強氧化性,能使蛋白質變性,故能殺菌消毒,故D正確.
故選C.
點評 本題考查了化學知識在生活中的應用,難度不大,應注意的是鈍化是反應程度很小的化學反應.


科目:高中化學 來源: 題型:選擇題
| A. | 在無色溶液中:NH4+、Fe2+、SO42-、CO32- | |
| B. | 在含大量Ba2+的溶液中:NH4+、Na+、Cl-、H+ | |
| C. | 在強堿溶液中:Na+、K+、Cl-、HCO3- | |
| D. | 在pH=1的溶液中:K+、Fe2+、Cl-、CH3COO- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 化學式 | 電離常數 |
| HClO | Ka=3×10-8 |
| H2CO3 | Ka1=4.3×10-7 |
| Ka2=5.6×10-11 |
| A. | c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3) | B. | c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-) | ||
| C. | c(HCO3-)>c(ClO-)>c(OH-) | D. | c(ClO-)>c(HCO3-)>c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鈉與水反應:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 稀硝酸中加入過量鐵粉:Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| C. | 鋁粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| D. | 氯氣與水反應:Cl2+H2O?H++Cl-+HClO |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電解精煉銅的過程中,鎂轉移NA個電子時,陽極溶解銅的質量為32g | |
| B. | 1molNa2O2固體中含離子總數為4NA | |
| C. | 1mol羥基與17g NH3所含電子數之比為9:10 | |
| D. | 1molNa2CO3晶體中含陰離子數小于1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
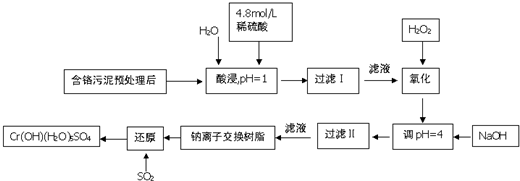
| 陽離子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 開始沉淀時的pH | 2.7 | 7.0 | - | - | - |
| 沉淀完全是的pH | 3.7 | 9.0 | 11.1 | 8 | 9(>9溶解) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電解稀硫酸制H2、O2時銅作陽極 | B. | 用電解法精煉粗銅時粗銅作陰極 | ||
| C. | 在鍍件上電鍍銅時用金屬銅作陰極 | D. | 銅鋅原電池中銅是正極 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com