
 隨著人類對溫室效應和資源短缺等問題的重視,如何降低大氣中CO2的含量及有效地開發利用CO2,引起了各國的普遍重視.
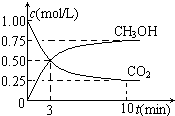
隨著人類對溫室效應和資源短缺等問題的重視,如何降低大氣中CO2的含量及有效地開發利用CO2,引起了各國的普遍重視.分析 (1)①在體積恒為1L的密閉容器中,充入1mol CO2和3mol H2,一定條件下合成甲醇,測得CO2和CH3OH(g)的濃度隨時間變化如圖所示.達到平衡時生成甲醇0.75mol/L×1L=0.75mol,放出熱量150kJ,生成1mol甲醇放熱=$\frac{150KJ}{0.75mol}×1mol$=200KJ,標注物質聚集狀態和對應反應焓變寫出熱化學方程式;
②由圖可知,10min到達平衡,平衡時甲醇的濃度變化為0.75mol/L,由方程式可知氫氣的濃度變化等于甲醇的濃度變化量3倍為2.25mol/L,根據v=$\frac{△c}{△t}$計算v(H2);
③化學平衡常數,是指在一定溫度下,可逆反應達到平衡時各生成物濃度的化學計量數次冪的乘積除以各反應物濃度的化學計量數次冪的乘積所得的比值;
④根據化學平衡狀態的特征解答,當反應達到平衡狀態時,正逆反應速率相等,各物質的濃度、百分含量不變,以及由此衍生的一些量也不發生變化,解題時要注意,選擇判斷的物理量,隨著反應的進行發生變化,當該物理量由變化到定值時,說明可逆反應到達平衡狀態;
⑤能使$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大,使平衡向正反應移動,注意不能增大二氧化碳或降低甲醇的量;
(2)陰極發生還原反應,CO2被還原生成CO,總反應式減去陽極反應式得陰極反應式;根據△G的大小判斷反應能否進行.
解答 解:(1)①在體積恒為1L的密閉容器中,充入1mol CO2和3mol H2,一定條件下合成甲醇,測得CO2和CH3OH(g)的濃度隨時間變化如圖所示.達到平衡時生成甲醇0.75mol/L×1L=0.75mol,放出熱量150kJ,生成1mol甲醇放熱=$\frac{150KJ}{0.75mol}×1mol$=200KJ,熱化學方程式為:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-200kJ/mol,
故答案為:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-200kJ/mol;
②由圖可知,10min到達平衡,平衡時甲醇的濃度變化為0.75mol/L,由方程式CO2(g)+3H2(g)?CH3OH(g)+H2O可知,氫氣的濃度變化等于甲醇的濃度變化量為0.75mol/L×3=2.25mol/L,故v(H2)=$\frac{2.25mol}{10min}$=0.225mol/(L•min),故答案為:0.225mol/(L•min);
③反應CO2(g)+3H2(g)?CH3OH(g)+H2O(g)的平衡常數K=$\frac{c(C{H}_{3}OH)c({H}_{2}O)}{c(C{O}_{2}){c}^{3}({H}_{2})}$,故答案為:$\frac{c(C{H}_{3}OH)c({H}_{2}O)}{c(C{O}_{2}){c}^{3}({H}_{2})}$;
④a.2個O-H鍵斷裂的同時,有3個H-H鍵斷裂,說明3mol氫氣消耗同時1mol水消耗,正逆反應速率相同,反應達到平衡狀態,故a正確;
b.反應前后氣體質量不變,氣體物質的量變化,當混合氣體平均相對分子質量不再改變,說明反應達到平衡狀態,故b正確;
c.反應速率之比等于化學方程式計量數之比,為正反應速率之比,正反應速率v(H2)=0.6mol/(L•min),逆反應速率v(CO2)=0.2mol/(L•min),說明二氧化碳的正逆反應速率相同,反應達到平衡狀態,故c正確;
d.反應前后氣體質量和體積不變,密度始終保持不變,不能說明反應達到平衡狀態,故d錯誤;
故答案為:a、b、c;
⑤能使$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大,使平衡向正反應移動,則.
A.該反應正反應是放熱反應,升高溫度平衡向逆反應移動,比值減小,故A錯誤;
B.充入He(g),使體系壓強增大,容器的容積不變,反應混合物的濃度不變,平衡不移動,比值不變,故B錯誤;
C.將H2O(g)從體系中分離,平衡向正反應移動,比值增大,故C正確;
D.再充入1mol CO2和3mol H2,等效為增大壓強,平衡向正反應移動,比值增大,故D正確;
故答案為:CD;
(2)總反應式為2CO2=2CO+O2,陽極反應為4OH--4e-=O2↑+2H2O,總反應式減去陽極反應式得陰極反應式,所以陰極反應為:2CO2+4e-+2H2O=2CO+4OH-,反應2CO=2C+O2(△H>0、△S<0),則△G=△H-T•△S>0,反應是一個焓增、熵減的反應,任何情況下不能自發進行;
故答案為:2CO2+4e-+2H2O=2CO+4OH-;不可行,該反應是一個焓增、熵減的反應,任何情況下不能自發進行.
點評 本題考查反應速率計算、化學平衡的影響因素、平衡常數等,題目難度中等,注意基礎知識的掌握,把握圖象的分析是解答的關鍵.


 探究與鞏固河南科學技術出版社系列答案
探究與鞏固河南科學技術出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | 醛基的電子式: | B. | 乙烯的結構簡式:CH2CH2 | ||
| C. | 尿素[CO(NH2)2]是一種有機物 | D. | 聚丙烯的化學式: |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO2使品紅、酸性高錳酸鉀溶液褪色,分別體現了它的漂白性和還原性 | |
| B. | 將Fe(NO3)2樣品溶于稀H2SO4后,滴加KSCN溶液,溶液變紅,說明Fe(NO3)2樣品已經變質 | |
| C. | 在未知溶液中滴加BaCl2溶液出現白色沉淀,加鹽酸,沉淀不溶解,說明該溶液中一定存在SO42- | |
| D. | 提純混有少量硝酸鉀的氯化鈉,應采用在較高溫度下制得濃溶液再冷卻結晶、過濾、干燥的方法 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | v(正)增大,v(逆)減小 | B. | v(正)減小,v(逆)增大 | ||
| C. | v(正)、v(逆)不同程度增大 | D. | v(正)、v(逆)同等程度增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
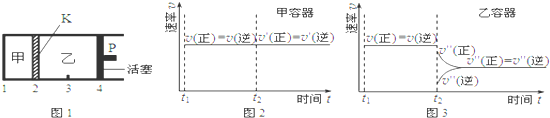
| A. | 保持活塞位置不變,降低溫度,達到新的平衡后,甲、乙中B的體積分數均增大 | |
| B. | 保持溫度和活塞位置不變,在甲中再加入1 mol A和2 mol B,達到新的平衡后,甲中C的濃度是乙中C的濃度的2倍 | |
| C. | 保持溫度和乙中的壓強不變,t2時分別向甲、乙中加入等質量的氦氣后,甲、乙中反應速率變化情況分別如圖2和圖3所示(t1前的反應速率變化已省略) | |
| D. | 保持溫度不變,移動活塞P,使乙的容積和甲相等,達到新的平衡后,乙中C的體積分數是甲中C的體積分數的2倍 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
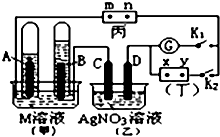 如圖所示的實驗裝置,丙為用淀粉碘化鉀和酚酞混合溶液潤濕的濾紙,m、n為夾在濾紙兩端的鉑夾.丁為直流電源,x、y為電源的兩極.G為電流計,電極均為石墨電極.閉合K2、斷開K1,一段時間后,A、B兩極產生的氣體體積之比為2:1,回答下列問題:
如圖所示的實驗裝置,丙為用淀粉碘化鉀和酚酞混合溶液潤濕的濾紙,m、n為夾在濾紙兩端的鉑夾.丁為直流電源,x、y為電源的兩極.G為電流計,電極均為石墨電極.閉合K2、斷開K1,一段時間后,A、B兩極產生的氣體體積之比為2:1,回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 紅棕色的NO2加壓后顏色先變深后變淺 | |
| B. | 鋼鐵在潮濕的空氣中容易生銹 | |
| C. | 溫度過高對合成氨不利 | |
| D. | 常溫下,將1mLpH=3的醋酸溶液加水稀釋至l00mL,測得其pH<5 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com