
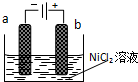
分析 (1)根據題意:制備Ni2O3的方法是電解NiCl2得Ni3+,在陽極上是Ni元素失電子的過程,據此判斷陽極材料;
(2)硫酸鈉是一種強電解質,溶液的導電能力強;
(3)根據電解池陰極上和陽極上的電極反應來判斷;
(4)電解過程中產生的Cl2在弱堿性條件下生成ClO-,把二價鎳氧化為三價鎳,據此書寫方程式;
(5)原電池的正極上發生得電子的還原反應,電解池的陰極上發生得電子的還原反應;
(6)原電池的負極發生氧化反應,電解池的陰極反應的逆反應是氧化反應,據此確定充電時,電極的連接情況.
解答 解:(1)根據題意:制備Ni2O3的方法是電解NiCl2得Ni3+,在陽極上是Ni元素失電子的過程,所以陽極材料是惰性電極材料,故答案為:C;
(2)硫酸鈉是一種強電解質,向其中加入硫酸鈉,是為了增加離子濃度,增強溶液的導電能力,故答案為:增加離子濃度,增強溶液的導電能力;
(3)電解過程中,陰極反應:2H++2e-=H2↑,促進水的電離,氫氧根離子濃度增大,該極附近溶液的pH升高,陽極反應:2Cl-2e-=Cl2↑,電解過程中陽極附近生成的氯氣與水反應生成鹽酸和次氯酸,溶液的pH降低,故答案為:升高;降低;
(4)電解過程中產生的Cl2在弱堿性條件下生成ClO-,把二價鎳氧化為三價鎳,即2Ni2++ClO-+H2O=2Ni3++Cl-+2OH-,故答案為:2Ni2++ClO-+H2O=2Ni3++Cl-+2OH-;
(5)①放電時,原電池的正極上發生得電子的還原反應Ni2O3+3H2O+2e-=2Ni(OH)2+2OH-,故答案為:Ni2O3+3H2O+2e-=2Ni(OH)2+2OH-;
②充電時,電解池的陰極反應的逆反應是氧化反應:Fe(OH)2+2e-=Fe+2 OH-,故答案為:Fe(OH)2+2e-=Fe+2 OH-;
(6)二次電池充電時,電池的負極和電源的負極相連,故答案為:負極.
點評 本題考查了原電池、電解池的知識,該考點是高考考查的重點和難點,側重于學生的分析能力的考查,本題有一定的綜合性,難度適中.


科目:高中化學 來源: 題型:解答題
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | ||
| 2 | ① | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | CH4、C2H4、C3H4 | |
| B. | CH4、C3H8、C2H2(C2H8、C2H2物質的量之比為1:3) | |
| C. | C2H6、C4H6、C2H2(物質的量之比為2:1:2) | |
| D. | C3H8、C4H8、C2H2(質量之比為11:14:26) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 轉移時沒有洗滌2~3次 | |
| B. | 定容時,俯視液面使之與刻度線相平 | |
| C. | 溶解時放出了大量的熱,但未等溫度恢復為常溫就開始轉移 | |
| D. | 轉移溶液前,容量瓶不干燥,留下少量的水 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 離子 | K+ | Na+ | NH4+ | SO42- | NO3-[] | Cl- |
| 濃度/mol?L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5[] | 3×10-5 | 2×10-5 |
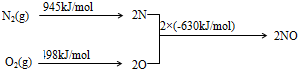
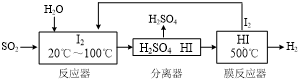
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④ | B. | ①② | C. | ②③ | D. | ②④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO2具有漂白性,能使滴有酚酞的NaOH溶液褪色 | |
| B. | Na2O2與水和二氧化碳反應都會生成氧氣,可用作供氧劑 | |
| C. | MgO、Al2O3熔點高,可用于耐高溫材料 | |
| D. | 常溫下,鋁與濃硝酸發生鈍化,可用鋁槽車貯運濃硝酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
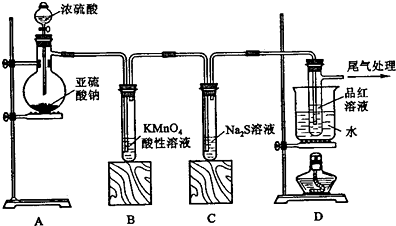
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

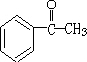 .
. .
. .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com