
| A. | 該溶液中一定不含Ba2+ | |
| B. | 該溶液中一定含Na+ | |
| C. | 無色氣體在標準狀況下的體積約為2.24L | |
| D. | 若向該溶液中加入足量NaOH溶液,濾出沉淀,洗凈灼燒后最多能得8.0g固體 |
分析 向該溶液中加入少量稀硫酸,無沉淀生成但有氣泡產生,說明溶液中一定不存在鋇離子,一定存在硝酸根離子和亞鐵離子,生成的氣體為一氧化氮;由于溶液中存在的4種離子的物質的量均為0.1mol,根據溶液電中性,溶液中一定還存在一種陰離子,若是存在氯離子,溶液已經呈電中性,不會存在其它離子,所以溶液中存在的陰離子為硫酸根離子,再根據溶液電中性可知,正電荷物質的量為:0.1mol×2=0.2mol,負電荷物質的量為:0.1mol×2+0.1mol=0.3mol,溶液中一定還存在0.1mol正電荷,該離子的物質的量為0.1mol,所以該離子為鈉離子.
解答 解:加入少量稀硫酸,無沉淀生成但有氣泡產生,說明一定不存在Ba2+,一定存在Fe2+、NO3-;根據溶液的電中性可以判斷溶液中還存在Na+、SO42-,
A.根據以上分析可知,溶液中一定不存在Ba2+,故A正確;
B.根據分析可知,該溶液中一定含Na+,故B正確;
C.根據反應方程式NO3-+3Fe2++4H+=NO↑+3Fe3++2H2O可知,亞鐵離子不足,加入足量的稀硫酸后,生成NO的總物質的量為:0.1mol×$\frac{1}{3}$=$\frac{1}{30}$mol,標況下體積為:22.4L/mol×$\frac{1}{30}$mol≈0.75L,故C錯誤;
D.若向該溶液中加入足量的NaOH溶液,充分反應后,過濾、洗滌、灼燒,最終所得固體為氧化鐵,根據鐵離子守恒,生成氧化鐵的物質的量為0.05mol,質量為:0.05mol×160g/mol=8.0g,故D正確;
故選C.
點評 本題考查離子的檢驗,題目難度中等,明確常見離子的性質及檢驗中發生的化學反應是解答本題的關鍵,注意檢驗中應排除離子的相互干擾來解答,并注意離子共存及溶電荷守恒的應用.


科目:高中化學 來源: 題型:多選題
| A. | H2O既不是氧化產物也不是還原產物 | |
| B. | 該反應中被氧化和被還原的氮元素的質量比是3:2 | |
| C. | 若有2mol NH3完全反應,共轉移12mol電子 | |
| D. | NO是氧化劑,NH3是還原劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0:1:12:11 | B. | 14:13:12:11 | C. | 14:13:2:3 | D. | 1:10:100:1000 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
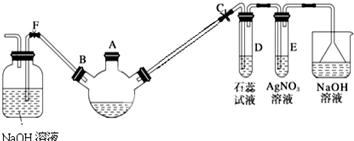
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
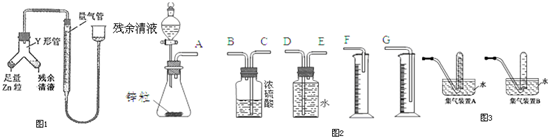
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗操作 | 實驗現象 | 結論 |
| A | 向盛有Fe(NO3)2溶液的試管中加入0.1mol•L-1硫酸溶液 | 試管口出現紅棕色氣體 | 溶液中NO3-被Fe2+還原為NO2 |
| B | H2S通入CuSO4溶液中 | 溶液中出現黑色沉淀 | 酸性:H2S>H2SO4溶液 |
| C | 在CuSO4溶液中加入KI溶液,再加入苯,振蕩、靜置 | 有白色沉淀生成,苯層呈紫紅色 | 白色沉淀可能為CuI |
| D | 將一小塊鈉投入到CuSO4溶液中 | 有無色無味的氣體放出,且出現藍色沉淀 | 氧化性:H+>Cu2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 實驗室需要0.1mol/LNaOH溶液500mL,根據這種溶液的配制情況回答下列問題.
實驗室需要0.1mol/LNaOH溶液500mL,根據這種溶液的配制情況回答下列問題.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 無機苯是由極性鍵組成的非極性分子 | |
| B. | 無機苯能發生加成反應和取代反應 | |
| C. | 無機苯不能使KMnO4酸性溶液褪色 | |
| D. | 無機苯的二氯取代物有3種同分異構體 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com