
分析 (1)根據氧化還原反應中,化合價升高數值=化合價降低值=轉移電子數,據電子守恒來配平方程式;
(2)在氧化還原反應中,得電子化合價降低的反應物是氧化劑,失電子化合價升高的反應物是還原劑,還原劑對應的產物是氧化產物;
(3)根據氯氣和轉移電子之間的關系式計算;
(4)根據原子守恒確定產物,結合反應產物來分析優(yōu)點.
解答 解:(1)氧化還原反應中,Cl化合價優(yōu)+5、+4、0、-1價,根據化合價不交叉的規(guī)律,+5價降為+4價,-1價升高為0價,化合價升高了2價,降低了1價,所以氯酸鈉前面是系數2,二氧化氯前邊系數是2,氯氣系數是1,根據Cl元素守恒,鹽酸系數是4,水前邊系數是2,
故答案為:2;4;2;2;1;2;
(2)該反應中,氯酸鈉中氯元素的化合價由+5價變?yōu)?4價,氯化氫中氯元素的化合價由-1價變?yōu)?價,所以氯酸鈉是氧化劑,鹽酸是還原劑,鹽酸中氯元素部分化合價不變,生成氯化鈉,顯示酸性,部分失電子作還原劑,
故答案為:NaClO3;還原性;酸性;
(3)根據氯氣和轉移電子之間的關系式得,反應中生成1mol氯氣轉移電子的物質的量是2mol,被氧化的鹽酸是2mol,有4.48L即0.2mol氯氣生成時,轉移的電子數為0.4mol,被氧化的鹽酸的物質的量為0.4mol,
故答案為:0.4;0.4;
(4)化學方程式是2NaClO2+Cl2═2ClO2↑+2A中,根據原子守恒,A的化學式為NaCl,該反應中不產生有毒的氯氣,可以減小對環(huán)境的污染,
故答案為:NaCl;不產生有毒的氯氣,減小對環(huán)境的污染.
點評 本題考查了氧化還原反應,明確元素化合價變化是解本題關鍵,注意知識的遷移應用,難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 從反應開始到建立平衡所需時間:tA>tB | |
| B. | 平衡時I2的濃度:c(I2)A=c(I2)B | |
| C. | 平衡時碘蒸氣在混合氣體中的百分含量:A容器大于B容器 | |
| D. | 平衡時HI的分解率:aA=aB |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化合反應 | B. | 分解反應 | C. | 置換反應 | D. | 復分解反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鈉鉀合金可用于中子反應堆作熱交換劑 | |
| B. | 氯氣本身有毒,因此不能用于藥物合成 | |
| C. | 不用氧化鎂電解熔融制鎂的原因是氧化鎂不導電 | |
| D. | 工業(yè)高爐煉鐵過程中,加石灰石主要是為了制備還原劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
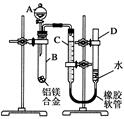 某學習小組用如圖所示裝置測定鋁鎂合金中鋁的質量分數和鋁的相對原子質量.
某學習小組用如圖所示裝置測定鋁鎂合金中鋁的質量分數和鋁的相對原子質量.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol過氧化鈉中陰離子數目為2NA | |
| B. | 1mol氯氣與足量的NaOH溶液反應,轉移電子的數目為2 NA | |
| C. | 標準狀況下,11.2L氨水含有0.5 NA個NH3分子 | |
| D. | 9g水中含有5 NA個電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
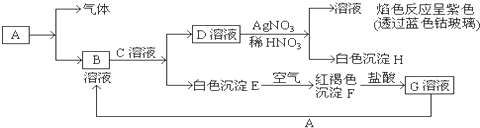
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 等質量的Na2CO3和NaHCO3分別與足量鹽酸反應,NaHCO3產生的CO2多 | |
| B. | 等物質的量的鹽酸分別與足量的Na2CO3和NaHCO3反應,Na2CO3產生的CO2多 | |
| C. | 相同溫度在水中的溶解度:Na2CO3大于NaHCO3 | |
| D. | 等物質的量的Na2CO3和NaHCO3分別與足量的鹽酸反應,消耗鹽酸的量一樣多 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
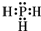 ;磷化氫具有強的還原性,通入硫酸銅溶液中會生成單質銅和磷酸,寫出該反應的離子方程式:PH3+4Cu2++4H2O=8H++H3PO4+4Cu.
;磷化氫具有強的還原性,通入硫酸銅溶液中會生成單質銅和磷酸,寫出該反應的離子方程式:PH3+4Cu2++4H2O=8H++H3PO4+4Cu.查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com