
分析 (1)根據離子氧化性Fe3+>Cu2+>Fe2+,鐵首先與鐵離子反應生成亞鐵離子,且無固體存在,說明溶液的銅離子沒參加反應,所以溶液中一定存在Cu2+和Fe2+;
(2)鐵粉有剩余,根據離子氧化性Fe3+>Cu2+>Fe2+,反應的反應方程式為:2FeCl3+Fe═3FeCl2、CuCl2+Fe═Cu+FeCl2,溶液中一定存在亞鐵離子,再根據方程式進行相關計算;
(3)當有銅生成,鐵粉無剩余,溶液中一定沒有Fe3+,Cu2+恰好全部參加反應或部分反應生成Fe2+和Cu,所以溶液中一定沒有Fe3+,可能含有Cu2+,一定含有Fe2+;如果只有Fe2+,則其物質的量為:0.7mol,如果還有Cu2+,且最多為0.2mol時,只發生2FeCl3+Fe=3FeCl2,則Fe2+物質的量為0.5mol,由于兩個反應都發生,所以Cu2+小于0.2mol,因此Fe2+物質的量大于0.5mol,故Fe2+物質的量為:0.5mol<n(Fe2+)≤0.7mol.
解答 解:(2)根據離子氧化性Fe3+>Cu2+>Fe2+,鐵首先與鐵離子反應生成亞鐵離子,且無固體存在,說明溶液的銅離子沒參加反應,所以溶液中一定存在Cu2+和Fe2+,故答案為:Cu2+和Fe2+;
(2)由于鐵粉有剩余,且氧化性Fe3+>Cu2+>Fe2+,所以溶液中Cu2+和Fe3+完全與鐵粉反應,所以過濾所得的固體物質為Cu和Fe;發生反應的方程式為:2FeCl3+Fe═3FeCl2、CuCl2+Fe═Cu+FeCl2,反應后溶液中只存在Fe2+,沒有Fe3+、Cu2+,根據氯離子守恒:n(Cl-)=(2mol/L×3+2mol/L×2+2mol/L×2)×0.1L=1.4mol,所以n(Fe2+)=$\frac{1}{2}$n(Cl-)=0.7mol,故答案為:Cu和Fe;0.7;
(3)當有銅生成,鐵粉無剩余,溶液中一定沒有Fe3+,Cu2+恰好全部參加反應或部分反應生成Fe2+和Cu,所以溶液中一定沒有Fe3+,可能含有Cu2+,一定含有Fe2+;如果只有Fe2+,則其物質的量為:0.7mol,如果還有Cu2+,且最多為0.2mol時,只發生2FeCl3+Fe=3FeCl2,則Fe2+物質的量為0.5mol,由于兩個反應都發生,所以Cu2+小于0.2mol,因此Fe2+物質的量大于0.5mol,故Fe2+物質的量為:0.5mol<n(Fe2+)≤0.7mol,故答案為:Fe2+;0.5 mol<n(Fe2+)≤0.7 mol.
點評 本題考查了Fe與Fe3+、Cu2+的反應,能正確判斷固體的成分是解本題的關鍵,根據固體的成分了解反應的先后順序,從而確定溶液的成分.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 陽離子和陰離子數目一定相等 | |
| B. | 陽離子帶的正電荷總數一定等于陰離子所帶的負電荷總數 | |
| C. | 除陰、陽離子外溶液中不會再有其它粒子 | |
| D. | 強電解質溶液的導電性一定強于弱電解質溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 密度/g•cm-3 | 沸點/℃ | 溶解性 | |
| 甲苯 | 0.866 | 110.6 | 不溶于水 |
| 對硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液態烴 |
| 鄰硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液態烴 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙醇在銅作催化劑的條件下加熱和空氣反應得乙醛 | |
| B. | 乙烯通入溴的四氯化碳溶液中的反應 | |
| C. | 在濃硫酸作用下,乙醇和乙酸共熱的反應 | |
| D. | 在濃硫酸作用下.苯在55℃左右與濃硝酸的反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
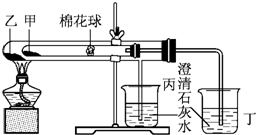 下列是某興趣小組根據課本實驗設計的一個能說明碳酸鈉與碳酸氫鈉熱穩定性的套管實驗.請觀察下圖的實驗裝置,分析實驗原理,回答下列問題:
下列是某興趣小組根據課本實驗設計的一個能說明碳酸鈉與碳酸氫鈉熱穩定性的套管實驗.請觀察下圖的實驗裝置,分析實驗原理,回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將一小塊鈉投入到盛有硫酸銅溶液的燒杯中,發現沒有紫紅色的銅析出,不能說明鈉的金屬性比銅弱 | |
| B. | 用濕潤的淀粉碘化鉀試紙放置在有氯氣產生的導管上端,發現試紙變藍,說明氯元素的非金屬性比碘元素強 | |
| C. | 把H2S氣體和Cl2在集氣瓶中混合,一段時間后發現瓶壁有淡黃色固體析出,說明Cl的非金屬性比S強 | |
| D. | 將0.1 mol Na、Mg、Al分別與足量稀鹽酸反應,金屬失去的電子數分別為0.1 mol、0.2 mol、0.3 mol,說明這三種金屬的活潑性為:Al>Mg>Na |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH4分子的比例模型: | B. | 氯原子的結構示意圖: | ||
| C. | NH3分子的電子式: | D. | CO2分子的結構式:O=C=O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 ,指出該化合物中的化學鍵離子鍵、非極性共價鍵.
,指出該化合物中的化學鍵離子鍵、非極性共價鍵. (6)請寫出元素G的基態原子電子排布式1s22s22p63s23p63d54s1.在CrCl3的水溶液中,一定條件下存在組成為[CrCln(H2O)6-n]x+(n和x均為正整數)的配離子,將其通過氫離子交換樹脂(R-H),可發生離子交換反應:
(6)請寫出元素G的基態原子電子排布式1s22s22p63s23p63d54s1.在CrCl3的水溶液中,一定條件下存在組成為[CrCln(H2O)6-n]x+(n和x均為正整數)的配離子,將其通過氫離子交換樹脂(R-H),可發生離子交換反應:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com