
| A. | 剩余固體是鐵、銅混合物 | |
| B. | 原固體混合物中銅的質量是6.4g | |
| C. | 反應后溶液中n(Fe3十)=0.l0mol | |
| D. | 反應后溶液中n(Fe2十)+n(Cu2十)=0.75mo1 |
分析 A.鐵的還原性強于銅,把鐵、銅混合粉末加入氯化鐵溶液中,先后發生:Fe+2Fe3+=3Fe2+、Cu+2Fe3+=Cu2++2Fe2+,溶液中n(FeCl3)=5mol/L×0.1L=0.5mol,計算0.5mol鐵離子完全反應,分別消耗Cu、Fe的質量,再根據參加反應的金屬質量判斷剩余固體的組成;
B.列方程計算參加反應的Cu、Fe物質的量,原固體混合物中Cu的質量=參加反應Cu的質量+剩余固體Cu的質量;
C.金屬有剩余,則Fe3+完全反應;
D.反應后溶液為FeC12、CuC12溶液,根據電荷守恒可知:n(Fe2+)+n(Cu2+)=$\frac{1}{2}$n(Cl-).
解答 解:A.鐵的還原性強于銅,把鐵、銅混合粉末加入氯化鐵溶液中,先后發生:Fe+2Fe3+=3Fe2+、Cu+2Fe3+=Cu2++2Fe2+,溶液中n(FeCl3)=5mol/L×0.1L=0.5mol,
設0.5mol鐵離子完全反應消耗Cu、Fe的質量分別為m1、m2,則:
Cu+2Fe3+=Cu2++2Fe2+ Fe+2Fe3+=3Fe2+
64g 2mol 56g 2mol
m1 0.5mol m2 0.5mol
m1=$\frac{64g×0.5mol}{2mol}$=16g,
m2=$\frac{56g×0.5mol}{2mol}$=14g,
溶解的金屬質量是18-3.2=14.8,則兩種金屬都參與反應,Fe3+完全反應,剩余的金屬是銅,故A錯誤;
B.設反應的銅的物質的量是n1 mol,反應的鐵物質的量為n2mol,則:
64n1+56n2=14.8
2n1+2n2=0.5
解得:n1=0.1,n2=0.15,
則原來含有的銅的質量是:0.1mol×64g/mol+3.2g=9.6g,故B錯誤;
C.金屬有剩余,則Fe3+完全反應,反應后溶液中沒有Fe3+,故C錯誤;
D.反應后溶液為FeC12、CuC12溶液,根據電荷守恒可知:n(Fe2+)+n(Cu2+)=$\frac{1}{2}$n(Cl-)=$\frac{0.5mol×3}{2}$=0.75mol;
故選:D.
點評 本題考查混合物的計算,側重于學生的分析能力和計算能力的考查,關鍵是明確發生反應先后順序及判斷反應剩余固體組成,難度中等.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
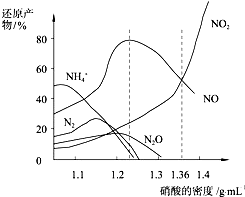
| A. | 密度小于1.1g/mL的硝酸與金屬反應,還原產物主要是NH4+ | |
| B. | 當硝酸溶液的密度為1.36g/mL時,Fe與過量硝酸反應的化學方程式為:4Fe+18HNO3=4Fe(NO3)3+3NO+3NO2+9H2O | |
| C. | 稀硝酸與金屬反應,一定被還原成NO | |
| D. | 某硝酸試劑瓶的標簽注明:密度1.26g/mL,質量分數50.0%;若取該試劑10mL配成1000mL溶液,所得溶液的物質的量濃度為1 mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 油脂發生皂化反應能生成甘油 | |
| B. | 蔗糖水解前后均可發生銀鏡反應 | |
| C. | Fe、Cu、Ag三種金屬常用化學還原劑還原法制得 | |
| D. | 向蛋白質溶液中加入CuSO4溶液發生鹽析 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 8.71g | B. | 8.86g | C. | 9.06g | D. | 7.04g |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 該物質屬于烴類 | B. | 該物質易溶于水 | ||
| C. | 該物質能使酸性高錳酸鉀溶液褪色 | D. | 該物質是一種高分子化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 衣料中的蠶絲和滌綸都屬于合成有機高分子材料 | |
| B. | 加碘食鹽和鐵強化醬油都可以補充人體必需的微量元素 | |
| C. | 建筑高樓大廈時用到的鋼是純凈物 | |
| D. | 用液化石油氣代替汽油作汽車燃料,不會造成空氣污染 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,6gO2和26gO3混合氣體中的原子總數為2NA | |
| B. | 100mL 0.1mol/L的NaCl溶液中,所含微粒總數為0.02NA | |
| C. | 23g金屬鈉變為鈉離子時得到的電子數為NA | |
| D. | 標準狀況下,2.24LH2O所含的原子數為0.3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(NH4+)相等的(NH4)2SO4溶液、NH4HSO4溶液和NH4Cl溶液中,溶質濃度大小關系是:c[(NH4)2SO4]<c[(NH4HSO4]<c(NH4Cl) | |
| B. | 欲除去CuCl2溶液中混有少量的FeCl3,可加入CuO | |
| C. | 0.2mol/L HCl溶液與等體積0.05mol/L Ba(OH)2溶液混合后,溶液的pH=1 | |
| D. | 0.2mol/L的NaHCO3溶液中c(H+)+c(H2CO3)=c(CO32-)+c(OH-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com