

分析 (1)①次氯酸鈣具有強的氧化性,能夠氧化鹽酸,生成氯化鈣、氯氣和水,依據化合價升級數目相同配平方程式;
②生成物中含有雜質氯化氫、水蒸氣;裝置C亦是安全瓶,監測實驗進行時D中是否發生堵塞,發生堵塞時C中的壓強增大,C中長頸漏斗中液面上升,形成水柱;
③可通過無水氯化鈣除去水蒸氣;
(2)根據固體表面積越大,反應速率越快;
(3)①蒸餾前若發現試管中液體呈黃色,說明含有氯氣,可以通過氯氣與錫花反應而除去;
②根據蒸餾裝置應通過溫度計控制溫度;根據四氧化錫(SnCl4)在潮濕的空氣中易水解,必須防止水的進入;
③根據收集的SnCl4中混有氯氣,氯氣有毒,可通過堿性溶液吸收;
解答 解:(1)①漂白粉固體和濃鹽酸反應生成氯化鈣、氯氣和水,化學方程式為:Ca(ClO)2+4HCl(濃)═CaCl2+2Cl2↑+2H2O;
故答案為:Ca(ClO)2+4HCl(濃)═CaCl2+2Cl2↑+2H2O;
②反應過程中氯化氫和水蒸氣是氯氣中的雜質,裝置B中飽和食鹽水的作用是除去Cl2中的HCl;裝置C亦是安全瓶,監測實驗進行時D中是否發生堵塞,發生堵塞時C中的壓強增大,C中長頸漏斗中液面上升,形成水柱;
故答案為:除去Cl2中的HCl;長頸漏斗中液面上升,形成水柱;
③生成物中含有雜質水蒸氣,可通過無水氯化鈣除去水蒸氣;
故答案為:無水氯化鈣;
(2)用錫花代替錫粒的目的是增大與氯氣的接觸面積,加快反應速率;
故答案為:增大與氯氣的接觸面積,加快反應速率;
(3)①蒸餾前若發現試管中液體呈黃色,說明含有氯氣,氯氣與錫花反應,可采取的措施是加入錫花;
故答案為:加入錫花;
②蒸餾裝置應通過溫度計控制溫度;四氧化錫(SnCl4)在潮濕的空氣中易水解,必須防止水的進入;該裝置匯總有兩處不合理之處,它們分別是缺少溫度計;Ⅱ和Ⅲ之間缺少干燥裝置;
故答案為:缺少溫度計;Ⅱ和Ⅲ之間缺少干燥裝置;
③收集的SnCl4中混有氯氣,氯氣有毒,可通過氫氧化鈉溶液吸收;
故答案為:氫氧化鈉溶液.
點評 本題考查了氯氣、四氧化錫的制備和性質,明確制備的原理和物質的性質是解題關鍵,注意題目信息的提取,題目難度中等.


科目:高中化學 來源: 題型:解答題
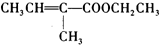 ;以化合物A為原料合成F的工藝流程如圖:
;以化合物A為原料合成F的工藝流程如圖:

 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 11.2L | B. | 22.4L | C. | 33.6L | D. | 44.8L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
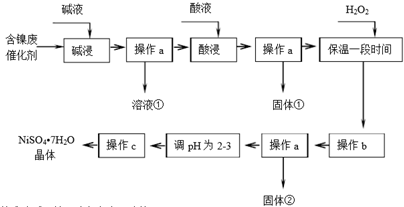
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 開始沉淀pH | 3.8 | 2.7 | 7.6 | 7.1 |
| 完全沉淀pH | 5.2 | 3.2 | 9.7 | 9.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 二甲醚是一種重要的清潔燃料,也可替代氟利昂作制冷劑等,對臭氧層無破壞作用.工業上可利用煤的氣化產物(水煤氣)合成二甲醚.請回答下列問題:
二甲醚是一種重要的清潔燃料,也可替代氟利昂作制冷劑等,對臭氧層無破壞作用.工業上可利用煤的氣化產物(水煤氣)合成二甲醚.請回答下列問題:| 物質 | CH3OH | CH3OCH3 | H2O |
| 濃度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 序號 | 氧化劑 | 還原劑 | 其他反應物 | 氧化產物 | 還原產物 |
| ① | Cl2 | FeBr2 | / | Cl- | |
| ② | KClO3 | 濃鹽酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| A. | 表中①組的反應只可能有一種元素被氧化和一種元素被還原 | |
| B. | 表②中若生成標準狀況下6.72LCl2,轉移電子數為0.6NA | |
| C. | 由表中①②組反應推測:ClO3-、Br-、H+、Fe2+不能在濃溶液中大量共存 | |
| D. | 表中③組反應的離子方程式為:2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com