
閱讀下表,綜合考慮表格各方面的因素,回答以下問題:
| 金屬 | 世界產量 /104 t | 密度 /103kg·m-3 | 熔點 /℃ | 導熱 性 | 導電 性 | 硬度 | 價格/ (元/噸) |
| 鋁 | 15 000 | 2.7 | 660 | 4 | 4 | 2~2.9 | 16 000 |
| 銅 | 8 000 | 8.9 | 1 083 | 2 | 2 | 2.5~3 | 17 700 |
| 金 | 2 | 19.3 | 1 064 | 3 | 3 | 2.5~3 | 9×108 |
| 鐵 | 301 430 | 7.9 | 1 535 | 8 | 7 | 4~5 | 2 200 |
| 鉛 | 3 000 | 11.3 | 327 | 9 | 9 | 1.5 | 4 900 |
| 銀 | 8 | 10.5 | 962 | 1 | 1 | 2.5~4 | 1 365 000 |
(注:表中導熱性能、導電性能和硬度數值由大到小,表明導熱、導電性能由弱到強;硬度由大到小。)
(1)導電性能最好的兩種金屬是 ,其中  更適合做導線,原因是 。
更適合做導線,原因是 。
(2)為什么炒菜時鋁鍋的鍋底容易變形而鐵鍋的鍋底卻不容易變形?
。
(3)鉛的密度較大,而鐮刀、錘子不能用鉛制的原因是
,
應選用的金屬是 。
科目:初中化學 來源: 題型:
為驗證質量守恒定律,某學習小組使用如圖所示的裝置進行實驗:
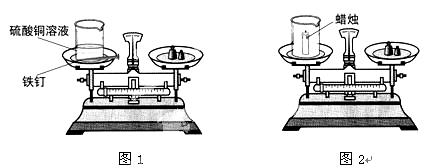
實驗一:如圖1,將盛有硫酸銅溶液的燒杯和用砂紙打磨干凈的鐵釘一起放在托盤天平上稱量,天平平衡后,將鐵釘浸到硫酸銅溶液中,一段時間后,觀察現象。
實驗二:如圖2,同學們又用此裝置做蠟燭在氧氣中燃燒實驗。
(1)實驗一中,學生觀察到溶液由藍色逐漸變成綠色,鐵釘表面有紅色物質析出,說明 ,實驗中還應觀察到的現象是 。
(2)實驗二中,學生沒有得出正確的實驗結論,分析原因并改進實驗方案。
查看答案和解析>>
科目:初中化學 來源: 題型:
下列措施有利于防止鐵制品銹蝕的是( )
A.農具上的鐵銹沒有及時除去
B.切過酸菜的菜刀不及時清洗
C.工地上的鋼管堆放在潮濕的地方
D.剪刀不用時涂上油并放在干燥處
查看答案和解析>>
科目:初中化學 來源: 題型:
下面是對鐵的銹蝕條件的探究。課本實驗中,鐵生銹所需要時間較長,某實驗小組設計了如圖所示的改進實驗。
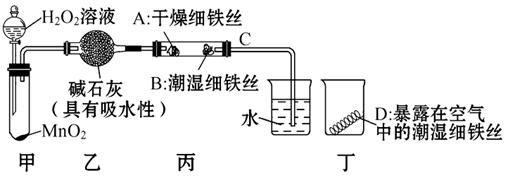
(1)檢查裝置的氣密性:連接好裝置,關閉分液漏斗的活塞,將C導管接入到裝有水的燒杯中,微熱甲裝置,說明氣密性良好的現象是
 。
。
(2)反應開始后,甲裝置中的反應現象:
,
MnO2的作用:
 。
。
(3)4分鐘后觀察:A處鐵絲依然光亮,B處鐵絲表面灰暗,D處鐵絲依然光亮,A、B處實驗現象對比,可得出鐵生銹與 有關;B、D處實驗現象對比說明:決定鐵生銹快慢的一個重要因素是
。
查看答案和解析>>
科目:初中化學 來源: 題型:
下列有關鐵的說法不正確的是( )
A.生鐵和鋼都是鐵合金
B.鐵是地殼中含量最多的金屬元素
C.工業煉鐵的原理是:3CO+Fe2O3 2Fe+3CO2
2Fe+3CO2
D.用鐵制作鐵鍋利用了鐵的導熱性
查看答案和解析>>
科目:初中化學 來源: 題型:
金屬材料在國防建設中起著重要的作用,圖1為殲﹣15飛機在航空母艦上起飛.
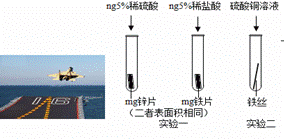
圖1 圖2
圖2
(1)國防建設中大量使用的是合金而不是純金屬,這是因為合金具有更多優良性能,例如鋁合金比純鋁的硬度 (填“大”或“小”).
(2)日常生活中鋁制品比鐵更耐腐蝕的原因是 (用化學方程式表示).
(3)鋼鐵的銹蝕主要是鐵與空氣中的 、 共同作用的結果.
(4)為了避免輪船的鋼質外殼被腐蝕,通常在輪船外殼上鑲嵌比鐵活動性強金屬.小明為探究鋅、鐵、銅三種金屬的活動性順序,設計了如圖2的兩個實驗:
①實驗一中,小明以“金屬表面產生氣泡的快慢”為標準來判斷鋅、鐵的活動性強弱,有同學認為不夠合理,理由是  .
.
②實驗二若出現 現象,可證明鐵的活動性強于銅.
(5)某興趣小組對一份含鐵的固體樣品進行探究.通過實驗已確定該樣品由氧化鐵和鐵粉混合而成.他們稱取了13.6g固體樣品,用圖3所示的裝置實驗,測定的數據如圖4所示.
①圖3中硬質玻璃管中的生成鐵的化學方程式為 .
②固體樣品中氧化鐵的質量是 克.
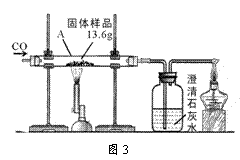
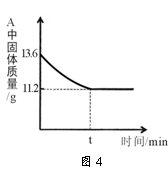
③將上述反應后11.2g的固體中加入100g稀鹽酸,恰好完全反應,求反應后所得溶液中溶質的質量分數 (結果精確到0.1%)(不寫計算過程).
查看答案和解析>>
科目:初中化學 來源: 題型:
精還原鐵粉是一種重要的化工原料,某興趣小組對其進行下列研究:
【物質制備】利用綠礬制備精還原鐵粉的工藝流程如下:
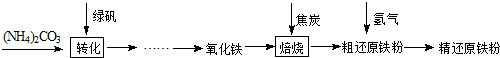
FexOy+yH2 xFe+yH2O Fe3C+2H2
xFe+yH2O Fe3C+2H2 3Fe+CH4粗還原鐵粉中還含有少量鐵的氧化物和Fe3C雜質,可用氫氣在高溫下進一步還原,其反應方程式為: .
3Fe+CH4粗還原鐵粉中還含有少量鐵的氧化物和Fe3C雜質,可用氫氣在高溫下進一步還原,其反應方程式為: .
(1)寫出焙燒中氧化鐵與CO反應的化學方程式 .
(2)焙燒中加焦炭的作用除了可以作燃料提供反應所需高溫外,還能 .
【含量測定】甲同學為得到精還原鐵粉并測定粗還原鐵粉中氧和碳元素的質量分數,按如下裝置進行實驗.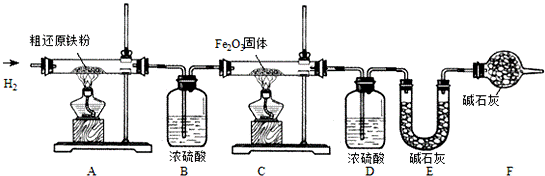
已知:3CH4+4Fe2O3 3CO2+6H2O+8Fe,濃硫酸有吸水性,堿石灰不僅能吸收水而且能吸收CO2.(假設每步反應都完全且不考慮裝置內原有空氣對測定結果的影響).
3CO2+6H2O+8Fe,濃硫酸有吸水性,堿石灰不僅能吸收水而且能吸收CO2.(假設每步反應都完全且不考慮裝置內原有空氣對測定結果的影響).
(3)主要實驗步驟如下:
①按順序組裝儀器,檢查裝置的氣密性,稱量樣品和必要裝置的質量;
②緩緩通入純凈干燥的H2;
③點燃C處酒精燈;
④點燃A 處酒精燈;
⑤分別熄滅A、C處酒精燈;
⑥ ;
⑦再次稱量必要裝置的質量.
(4)步驟②的目的是 ,驗證該步驟目的達到的實驗方法是 .
(5)反應后C裝置中的現象是 .
(6)裝置F的作用是 .
(7)若缺少裝置D,則所測氧元素的質量分數將 (“偏大”、“偏小”或“不變”).
(8)實驗后,甲同學根據裝置 (填A、B、C、D、E、F)的增重分別算得樣品中氧和碳元素的質量分數.
(9)乙同學將10.0克粗還原鐵粉樣品與足量稀鹽酸充分反應,經測定共產生0.3克氣體.計算該粗還原鐵粉樣品中鐵單質的質量分數.(要求寫出計算過程)
查看答案和解析>>
科目:初中化學 來源: 題型:
汽油屬于易燃物,敞口放置一瓶汽油,雖然與空氣接觸,但并未燃燒,這是由于
( )
A.汽油具有揮發性
B.汽油的著火點較低
C.與汽油接觸的氧氣少
D.周圍環境溫度低于汽油的著火點
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com