
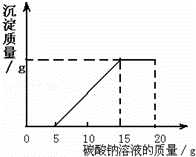
王強同學在完成制取二氧化碳的實驗后,對回收的鹽酸和氯化鈣混合溶液(不含其它的雜質)進行如下實驗:取一定量該混合溶液放入燒杯中,再滴入20g溶質質量分數為10.6%的碳酸鈉溶液.滴入碳酸鈉溶液的質量與生成沉淀的質量的關系如圖所示.
(1)剛加入碳酸鈉溶液時,發現沒有沉淀生成,卻有氣泡產生,原因是 (用化學方程式表示).
(2)計算反應中生成氣體的質量.
(3)計算所取混合液中CaCl2的質量.
| 根據化學反應方程式的計算.. | |
| 專題: | 綜合計算(圖像型、表格型、情景型計算題). |
| 分析: | 由圖中數據可知與混合液中HCl反應、與混合液中氯化鈣反應的碳酸鈉溶液的質量. 由與混合液中HCl反應的碳酸鈉溶液的質量根據碳酸鈉與稀鹽酸反應的化學方程式可以計算出生成氣體的質量. 根據氯化鈣與碳酸鈉反應的化學方程式可以計算出氯化鈣的質量. |
| 解答: | 解:(1)剛加入碳酸鈉溶液時,發現沒有沉淀生成,卻有氣泡產生,是碳酸鈉與稀鹽酸反應生成了氯化鈉和水和二氧化碳; (2)由圖中數據可知與HCl反應的碳酸鈉溶液的質量為5g. 設生成氣體的質量為x. Na2CO3+2HCl=2NaCl+H2O+CO2↑ 106 44 5g×10.6% x
x=0.22g (2)由圖中數據可知與氯化鈣反應的碳酸鈉溶液的質量為15g﹣5g=10g. 設混合液中氯化鈣的質量為y. Na2CO3+CaCl2=CaCO3↓+2NaCl 106 111 10g×10.6 y
y=1.11g 答案:(1)2HCl+Na2CO3═2NaCl+CO2↑+H2O; (2)生成氣體的質量為0.22g; (3)混合液中氯化鈣的質量為1.11g. |
| 點評: | 本題主要考查有關化學方程式的計算和溶質質量分數的計算,難度較大. |


科目:初中化學 來源: 題型:
邏輯推理是一種重要的化學思維方法,以下推理合理的是( )
|
| A. | 堿性溶液能使酚酞試液變紅,滴入酚酞試液后變紅的溶液一定呈堿性 |
|
| B. | 鋅和銅均是金屬,鋅與稀硫酸反應生成氫氣,則銅也能與稀硫酸反應生成氫氣 |
|
| C. | 某氣體不能使帶火星的木條復燃,所以該氣體一定不含氧氣 |
|
| D. | 化合物都是由不同元素組成的,不同元素組成的物質一定是化合物 |
查看答案和解析>>
科目:初中化學 來源: 題型:
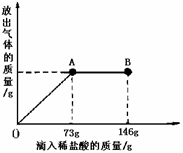 已知 Na2CO3的水溶液呈堿性,在一燒杯中盛有20.4g Na2CO3和NaCl 組成的固體混合物。向其中逐漸滴加溶質質分數為10%的稀鹽酸。放出氣體的總質量與所滴入稀鹽酸的質量關系曲線如下圖所示,請根據題意回答問題:
已知 Na2CO3的水溶液呈堿性,在一燒杯中盛有20.4g Na2CO3和NaCl 組成的固體混合物。向其中逐漸滴加溶質質分數為10%的稀鹽酸。放出氣體的總質量與所滴入稀鹽酸的質量關系曲線如下圖所示,請根據題意回答問題:
(1)當滴加稀鹽酸至圖中B點時,燒杯中溶液的pH ▲ 7(填>、=、<)。
(2)原混合物中碳酸鈉的質量。
(3)當滴加稀鹽酸至圖中A點時,燒杯中為不飽和溶液,通過計算求出其中溶質的質量分數。(計算結果保留一位小數)
查看答案和解析>>
科目:初中化學 來源: 題型:
某學習小組在做氫氣還原氧化銅的實驗時,在試管內加入氧化銅固體10克,通入氫氣一會兒后再給氧化銅加熱,反應完全后撤去酒精燈并停止通入氫氣,在空氣中將試管冷卻,發現部分紅色團體又變回黑色.稱得試管中剩余固體質量為8.4克.
(1)“在空氣中將試管冷卻”會導致 ,使“部分紅色固體又變回黑色”.
(2)按此實驗操作及獲得的數據,可知試管剩余固體中有氧化銅 克.
查看答案和解析>>
科目:初中化學 來源: 題型:
下列有關構成物質粒子的說法,正確的是( )
A.分子、原子能直接構成物質,離子不能直接構成物質
B.分子一定比原子大
C.原子中一定含有質子、中子、電子三種粒子
D.原子質量主要集中在原子核上
查看答案和解析>>
科目:初中化學 來源: 題型:
研究氧氣的性質,我們知道①木炭 ②硫 ③磷 ④鐵等物質都能在純氧中燃燒。
(1)請你寫出上述四個反應的化學符號表達式:
① ; ② ;
③ ; ④ 。
其中鐵在氧氣中燃燒的主要現象為_________ ______________________ _.
______________________ _.
(2)從不同角度來分析 ,上述反應都有許多相似之處。請在橫線處填寫完整:
,上述反應都有許多相似之處。請在橫線處填寫完整:
①示例:從物質類別分析,上述反應的反應物和生成物每一種都是純凈物。
②從化學反應的能量變化分析,都會 熱量(填“放出或吸收”)。
③從化學反應的基本類型分析,都屬于 反應。(填化合反應或分解反應)
查看答案和解析>>
科目:初中化學 來源: 題型:
下列關于O2的說法不科學的是( )
|
| A. | 常用帶火星的木條來檢驗空氣中的O2 |
|
| B. | 硫在O2里燃燒產生明亮的藍紫色火焰 |
|
| C. | 工業上將空氣液化后再進行分離來制取O2 |
|
| D. | 加熱KClO3制O2,可用MnO2作催化劑 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com