
| A. | 一定量氧化鐵與氧化銅的混合物與50g溶質的質量分數為14.6%的稀鹽酸,恰好完全反應,則原混合物中氧元素的質量一定是0.6g | |
| B. | 可以用聞氣味的方法區分碳酸氫銨和磷礦粉兩種化肥 | |
| C. | 當飽和溶液析出晶體后,剩余溶液中溶質的質量分數一定減少 | |
| D. | 將2.4g鎂、鋁合金(不含其他物質)與足量的稀硫酸充分反應后,生成0.2g H2 |
分析 A、根據氧化鐵和氧化銅與稀鹽酸反應的化學方程式結合氯化氫的質量,根據氧元素的質量守恒分析解答.
B、根據碳酸氫銨有刺激性氣味,磷礦粉沒有進行分析.
C、根據飽和溶液析出晶體可能是采用恒溫蒸發溶劑的方法,進行分析判斷.
D、根據等質量的鎂、鋁與足量稀硫酸反應時,鋁產生的氫氣多進行分析.
解答 解:A、氧化物中氧元素全部轉變為水中的氧元素,計算出水的質量進而計算出所含氧元素的質量即可;
設生成水的質量是x,氯化氫與生成水的關系為
2HCl~~~H2O
73 18
50g×14.6% x
$\frac{73}{18}$=$\frac{50g×14.6%}{x}$,x=1.8g
所以水中氧元素的質量為:1.8g×$\frac{16}{18}$×100%=1.6g.故錯誤.
B、碳酸氫銨有刺激性氣味,磷礦粉沒有,氣味不同,聞氣味可以鑒別,故正確.
C、飽和溶液析出晶體可能是采用恒溫蒸發溶劑的方法,由于溫度不變,得到的仍是該溫度下的飽和溶液,剩余溶液中溶質的質量分數不變,故選項說法錯誤.
D、等質量的鎂、鋁與足量稀硫酸反應時,鋁產生的氫氣多,2.4g鎂與足量的稀硫酸充分反應后,能生成0.2g 氫氣,因此將2.4g鎂、鋁合金(不含其他物質)與足量的稀硫酸充分反應后,生成氫氣的質量大于0.2g,故說法錯誤.
故選B.
點評 此題難度不大,掌握質量守恒定律、鑒別物質的方法以及溶液的有關知識等即可順利解答.


科目:初中化學 來源: 題型:選擇題
| A. | 用小蘇打作發酵粉焙制糕點 | B. | 用甲醛溶液浸泡海產品 | ||
| C. | 用亞硝酸鈉代替食鹽做調味劑 | D. | 把霉變大米淘凈后繼續食用 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 硫 | B. | 木炭 | C. | 紅磷 | D. | 蠟燭 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
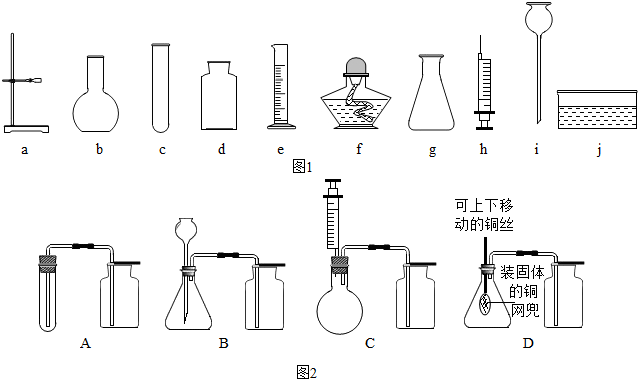
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 4Al+3O2═2Al2O3 | B. | CH4+2O2═CO2+2H2O | ||
| C. | 2KMnO4═K2MnO4+MnO2+O2↑ | D. | 2H2+O2═2H2O |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
| 實驗步驟 | 實驗現象 | 實驗結論 |
| 猜想③成立 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 任意比 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com