
教材上有一習題:“設計實驗證明甲烷中含有氫元素和碳元素。”現有一瓶用排水法收集到的甲烷氣體(圖1中的A)。請根據圖中裝置完成以下各題:

(1)要將A中的氣體通入B裝置中,應選圖2中的_________(填序號)“注水裝置”。
(2)B處是干冷的大燒杯,甲烷燃燒后燒杯內壁有水霧出現,證明甲烷中一定含有_____元素;將B中燒杯正放向其中滴加澄清石灰水,出現渾濁,證明甲烷中一定含有_______元素。
(3)此實驗能否證明甲烷分子中是否含有氧元素_________(填“能”或“不能”)。
 (4)寫出甲烷燃燒的化學方程式_________________________________________。
(4)寫出甲烷燃燒的化學方程式_________________________________________。
科目:初中化學 來源: 題型:
長期飲用純凈水不利于人體健康,如今很多家庭開始使用直飲機,機身內部結構采用“活性炭+超濾膜+紫外線”的組合工藝獲得直飲水,活性炭起 作用;用紫外線代替氯氣對水進行處理,其作用是 ;欲檢驗經過直飲機后的水是硬水還是軟水,應加入少量 ,若觀察到 ,則為軟水.
查看答案和解析>>
科目:初中化學 來源: 題型:
取少量碳酸氫鈉(NaHCO3)粉末,用如圖裝置進行實驗,充分加熱后發現,大試管中管口有水珠出現,管底有白色固體殘留;小試管中澄清石灰水變渾濁,完全反應后,取殘留固體溶于水配成溶液,往該溶液中滴加CaCl2溶液,有白色沉淀生成。

(1)小試管中澄清石灰水變渾濁,說明碳酸氫鈉受熱有 生成(填化學式)。
(2)通過上述實驗,下列歸納出的碳酸氫鈉性質或推理正確的有 (填編號)
A.NaHCO3能與NaOH溶液發生反應
B.NaHCO3受熱易分解:2NaHCO3 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.加熱時NaHCO3比Na2CO3易分解
D.無法比較NaHCO3與Na2CO3受熱分解的難易程度
查看答案和解析>>
科目:初中化學 來源: 題型:
在研究酸和堿的化學性質時,某小組想證明稀硫酸和氫氧化鈉溶液混合后,雖然無明顯現象,但確實發生了化學反應。試與他們一起完成實驗方案的設計、實施和評價,并得出有關結論。
(1)探究稀硫酸和氫氧化鈉溶液的反應:
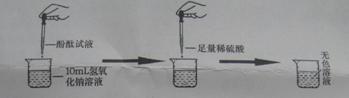 當滴入幾滴酚酞試液后,溶液由無色變為 色。根據上述實驗中顏色變化,可確定稀硫酸和氫氧化鈉溶液發生了化學反應,反應的化學方程式為: ;
當滴入幾滴酚酞試液后,溶液由無色變為 色。根據上述實驗中顏色變化,可確定稀硫酸和氫氧化鈉溶液發生了化學反應,反應的化學方程式為: ;
(2)探究上述稀硫酸和氫氧化鈉溶液反應后燒杯中的硫酸是否過量:
根據上述反應過程中溶液變成無色,不能確定稀硫酸是否過量。同學們又分別選取氯化鋇溶液、紫色石蕊試液設計實驗方案,請你判斷并分析:
| 實驗方案 | 實驗步驟 | 實驗現象 | 實驗結論 |
| 方案一 | 取樣,滴入適量的氯化鋇溶液 | 出現白色沉淀 | 稀硫酸過量 |
| 方案二 | 取樣,滴入幾滴紫色石蕊試液 | 溶液變紅 | 稀硫酸過量 |
上述設計的實驗方案中,正確的是 (填“方案一”或“方案二”);
另外一個實驗方案錯誤的原因是 ;
若請你再設計一個確定稀硫酸是否過量的實驗方案,你選用的藥品是 ,實驗現象及結論是 。
查看答案和解析>>
科目:初中化學 來源: 題型:
某同學用氫氧化鈣和鹽酸進行酸堿中和反應的實驗時,向燒杯中的氫氧化鈣溶液中滴加稀鹽酸一會兒后,發現忘記了滴加指示劑,因此,他停止滴加稀鹽酸,并對燒杯內溶液中的溶質成分進行了如下探究。請你和他一起完成探究活動。
【提出問題】溶液中的溶質是什么物質?
【作出猜想】猜想一:溶液質只有氯化鈣。
猜想二:溶質中有CaCl2和Ca(OH)2。
猜想三:溶液中有
【查閱資料】氯化鈣溶液呈中性。
【方案設計】
| 方案 | 方法步驟 | 實驗現象 | 實驗結論 |
| 方案一 | 取少量燒杯內的溶液于試管中,滴入幾滴無色酚酞溶液 | 酚酞不變色 | 猜想一正確 |
| 酚酞變紅色 | 猜想二正確 | ||
| 方案二 | 取少量燒杯內的溶液于試管中,逐滴加入 溶液至過量 |
| 猜想三正確 |
【方案評價】該同學與同學們通過討論后認為:(1)方案一能證明猜想二正確,但不能證明猜想一正確。(2)方案二可行,但該同學在記錄時未記錄完整,請你替他將方案二補充完整。
【方案反思】方案一不能證明猜想一正確的理由是 。
【拓展與應用】實驗證明猜想三是正確的。要想使溶液中的溶質只有氯化鈣,你認為應該進行的實驗步驟是 。
【結論】在分析化學反應后所得物質的成分時,除考慮生成物外還需考慮 。
查看答案和解析>>
科目:初中化學 來源: 題型:
氫化鈣固體是登山運動員常用的能源提供劑.某探究小組的同學通過查閱資料得知,氫化鈣(CaH2)遇水反應生成氫氧化鈣和氧氣.探究小組的同學把一定量的CaH2加入Na2CO3溶液中,充分反應后過濾,得到濾渣和濾液.經檢驗濾渣的成分是碳酸鈣.
【提出問題】濾液中溶質的成分是什么?
【猜想與假設】
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
經過討論,大家一致認為猜想四不合理,請用化學方程式說明原因 __________________【實驗驗證】
 【反思與拓展】①若向NH4Cl的溶液中加一定量CaH2,充分反應,產生的氣體是 _______;②登山運動員常用CaH2作為能源提供劑,與氫氣相比,其優點是__________________。
【反思與拓展】①若向NH4Cl的溶液中加一定量CaH2,充分反應,產生的氣體是 _______;②登山運動員常用CaH2作為能源提供劑,與氫氣相比,其優點是__________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
某興趣小組在做完碳還原氧化銅實驗后,進行了題23圖所示的探究:
 題23圖
題23圖
【猜想】把氧化銅還原成銅的物質是:I.石墨棒;II· 。
【實驗】用天平稱量1.5g氧化銅粉末,直接用鋁箔紙包裹。按上述操作步驟實驗,黑色粉末. ,那么猜想Ⅱ不成立。
【結論】石墨棒能使氧化銅還原成銅,該反應的化學方程式為 。
【改進】把石墨棒換成鋁粉,重復上述操作,又獲成功。那么,稱取等量的鋁粉并進行同樣
的操作,其目的是 。改進后的實驗證明,金屬鋁與銅活動性順序是
. ,該反應的化學方程式為 。
【拓展】如果使用復印機的“碳粉”代替石墨棒還原氧化銅,效果更好。聯想在空氣中灼熱
的鐵絲不能燃燒,而鐵粉能燃燒,其原因是 。
查看答案和解析>>
科目:初中化學 來源: 題型:
研究性學習小組測定實驗室里一瓶久置的NaOH固體是否變質。
【提出問題】NaOH固體是否變質?
【猜想與假設】猜想1:沒變質,全部是NaOH;
猜想2:完全變質,全部是Na2CO3;
猜想3:部分變質,既含有NaOH又含有Na2CO3。
【設計方案并進行實驗】請你與他們一起完成,并回答所給問題。
| 實驗步驟 | 實驗現象 | 實驗結論 |
| ①稱取上述固體樣品8g溶于100mL水配成溶液,向溶液中滴加過量的氯化鈣溶液,充分反應后,靜置。 | _________ _________ | 說明固體中一定含有Na2CO3 |
| ②用玻璃棒蘸取少量①中的上層清液滴在pH試紙上,與標準比色卡對比,測出pH | pH=10 | 說明固體中還一定含有__________(填化學式) |
上述步驟①中,滴加過量氯化鈣溶液的目的是_____________________________。
【實驗結論】通過實驗,說明上述猜想_____________是正確的。
【拓展】(1)為測定出該NaOH固體的變質程度,繼續將上述白色沉淀過濾、洗滌、干燥、稱得其質量為2g,則原固體樣品中NaOH的質量分數為______________(假定固體中無其它雜質)。
(2)要除去氫氧化鈉中含有的碳酸鈉,所用的方法(用化學方程式表示)__________________________________。
【反思】通過實驗,實驗室中的氫氧化鈉應密封保存。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com