
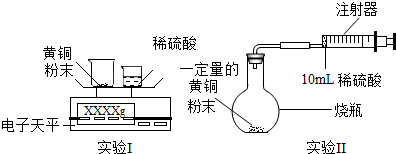
| 時間/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器讀數/mL | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
分析 (1)黃銅中的銅不能和稀硫酸反應,鋅能和稀硫酸反應生成硫酸鋅和氫氣;
(2)凡是有氣體參加或產生的實驗,實驗前一定要檢查裝置的氣密性,以防裝置漏氣影響實驗結果;
若稀硫酸是緩慢推入的,稀硫酸和鋅反應生成的氫氣會導致燒瓶內氣壓增大,稀硫酸難以完全推入燒瓶中或儀器連接處脫落,影響實驗;
(3)實驗I反應前后的質量差即為反應生成氫氣的質量;
(4)根據表中提供的數據可以判斷反應生成氫氣的體積;
(5)根據氫氣的密度和體積可以計算氫氣的質量,根據氫氣的質量和反應的化學方程式可以計算黃銅中鋅的質量,進一步可以計算出該黃銅中鋅的質量分數;
(6)銅和金不能和稀鹽酸、稀硫酸反應,鋅能和稀鹽酸反應生成氯化鋅和氫氣;
在酒精燈火焰上加熱時,金無明顯現象,而黃銅中的銅能和空氣中的氧氣反應生成黑色固體氧化銅.
解答 解:(1)實驗I中,將小燒杯中的所有稀硫酸分幾次加入到大燒杯中時,黃銅中的鋅和稀硫酸反應生成硫酸鋅和氫氣,產生氣泡,當鋅完全反應后,不再產生氣泡,因此判斷大燒杯中藥品完全反應的實驗現象是不再產生氣泡.
故填:不再產生氣泡.
(2)實驗II中,實驗操作是:先連接好裝置,再檢查裝置氣密性,該操作的具體方法是:將注射器活塞向內(左)推動一段距離,松手后注射器活塞回到原來的位置,說明裝置不漏氣;
最后將10mL稀硫酸快速推入燒瓶中,若稀硫酸是緩慢推入的,稀硫酸和鋅反應生成的氫氣會導致燒瓶內氣壓增大,則可能造成的后果是燒瓶內氣壓增大,稀硫酸難以完全推入燒瓶中或儀器連接處脫落.
故填:檢查裝置氣密性;將注射器活塞向內(左)推動一段距離,松手后注射器活塞回到原來的位置;燒瓶內氣壓增大,稀硫酸難以完全推入燒瓶中或儀器連接處脫落.
(3)反應前總質量已知,如果知道小燒杯的質量、大燒杯和反應后剩余物的總質量,則大燒杯和反應后剩余物的總質量與小燒杯的質量和與反應前總質量的差即為反應生成氫氣的質量,因此要計算生成H2的質量,至少還需要的數據是m(小燒杯)、m(大燒杯+反應后剩余物).
故填:AC.
(4)反應前注射器讀數是10mL,反應后最終讀數是90.0mL,因此最終生成H2的體積是:90.0mL-10mL=80.0mL.
故填:80.0.
(5)反應生成氫氣質量為:0.09g/1000mL×80.0mL=0.0072g,
設黃銅中鋅的質量為x,
Zn+H2SO4═ZnSO4+H2↑,
65 2
x 0.0072g
$\frac{65}{x}$=$\frac{2}{0.0072g}$,
x=0.234g,
該黃銅中鋅的質量分數為:$\frac{0.234g}{5g}$×100%=4.7%,
故填:4.7%.
(6)因為銅和金不能和稀鹽酸、稀硫酸反應,鋅能和稀鹽酸反應生成氯化鋅和氫氣,在酒精燈火焰上加熱時,金無明顯現象,而黃銅中的銅能和空氣中的氧氣反應生成黑色固體氧化銅,因此區別黃銅和黃金的方法是:方法一:分別向黃銅和黃金上滴加稀鹽酸或稀硫酸,產生氣泡的是黃銅,不產生氣泡的是黃金;
方法二:取黃銅和黃金分別在酒精燈火焰上灼燒,表面變黑的是黃銅,無明顯現象的是黃金.
故填:方法一:分別向黃銅和黃金上滴加稀鹽酸或稀硫酸,產生氣泡的是黃銅,不產生氣泡的是黃金;
方法二:取黃銅和黃金分別在酒精燈火焰上灼燒,表面變黑的是黃銅,無明顯現象的是黃金.
點評 實驗現象是物質之間相互作用的外在表現,因此要學會設計實驗、觀察實驗、分析實驗,為揭示物質之間相互作用的實質奠定基礎.


科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 乙>甲>丙 | B. | 甲>丙>乙 | C. | 丙>乙>甲 | D. | 乙>丙>甲 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
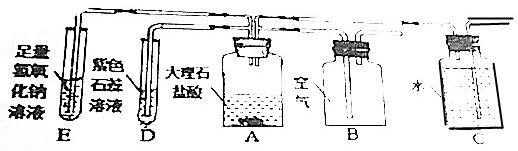
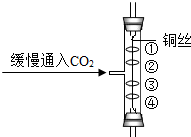 如圖所示實驗中,①、④為用紫色石蕊溶液潤濕的棉球,②③為浸過紫色石蕊溶液的干燥棉球.下列能準確描述實驗現象的是( )
如圖所示實驗中,①、④為用紫色石蕊溶液潤濕的棉球,②③為浸過紫色石蕊溶液的干燥棉球.下列能準確描述實驗現象的是( )| A. | ①變紅,③不變紅 | B. | ④變紅,③不變紅 | ||
| C. | ①、④變紅,②、③不變紅 | D. | ④比①先變紅,②、③不變紅 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 用紅磷測定空氣中氧氣含量的實驗,紅磷量不足導致所得結果偏大 | |
| B. | 配制5%的氯化鈉溶液時,量取水仰視讀數,會導致溶液的質量分數偏大 | |
| C. | 一定量的過氧化氫溶液制取氧氣,所用二氧化錳的量越多,制得的氧氣質量越大 | |
| D. | 某溶液能使紫色石蕊溶液變紅一該溶液的pH一定小于7 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com