
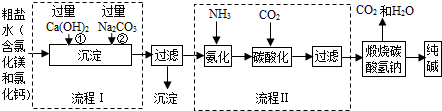
分析 (1)根據碳酸鈉的作用進行解答;根據氫氧化鈣和氯化鎂反應,碳酸鈉和氯化鈣反應進行解答;
(2)根據工業制純堿的反應進行解答;
(3)根據碳酸氫鈉受熱分解生成物為碳酸鈉、水和二氧化碳分析;
(4)根據氨氣溶于水溶液顯堿性,有利于二氧化碳的吸收進行解答;
(5)根據該溫度下碳酸氫鈉的溶解度比氯化銨小進行解答
解答 解:(1)流程圖Ⅰ是依次向粗鹽水中加入Ca(OH)2和Na2CO3,二者加入的順序不能顛倒,如果顛倒,過量的氫氧化鈣和新生成的氯化鈣無法除去;氫氧化鈣和氯化鎂反應生成氫氧化鎂沉淀和氯化鈣,碳酸鈉和氯化鈣反反應生成碳酸鈣沉淀和氯化鈉,過濾Ⅰ得到的沉淀成分有:氫氧化鎂和碳酸鈣;
(2)根據氯化鈉、水、氨氣和二氧化碳反應生成碳酸氫鈉和氯化銨,發生的總反應NaCl+H2O+NH3+CO2═NaHCO3+NH4Cl;
(3)碳酸氫鈉受熱分解生成物為碳酸鈉、水和二氧化碳,化學方程式為2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;
(4)氨氣溶于水溶液顯堿性,有利于二氧化碳的吸收;
(5)工業生產純堿的流程中,碳酸化時溶液中析出碳酸氫鈉而沒有析出氯化銨的原因是在該溫度下碳酸氫鈉的溶解度比氯化銨小.
故答案為:(1)不能顛倒,如果顛倒,過量的氫氧化鈣和新生成的氯化鈣無法除去;氫氧化鎂和碳酸鈣;
(2)NaCl+H2O+NH3+CO2═NaHCO3+NH4Cl;
(3)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;
(4)增大二氧化碳的吸收量;
(5)在該溫度下碳酸氫鈉的溶解度比氯化銨小.
點評 本題考查利用課本知識解決新問題能力,能加深學生對課本知識的理解,訓練學生的思維能力.


 浙江名校名師金卷系列答案
浙江名校名師金卷系列答案 全優沖刺100分系列答案
全優沖刺100分系列答案科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
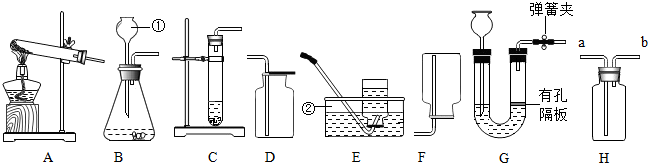
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
| 項目 | 標準 |
| 感官指標 | 無異味、異臭等 |
| 化學指標 | pH6.5-8.5,銅<1.0mg•L-1,鐵<0.3mg•L-1,氟化物<1.0mg•L-1,游離氯≥0.3mg•L-1等 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
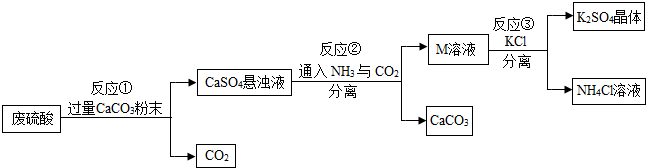
| 物質 | KCL | K2SO4 | NH4Cl | (NH4)2SO4 |
| 溶解度/g(20℃) | 34.2 | 11.1 | 37.2 | 75.4 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
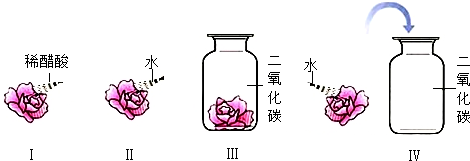
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
| 物質的質量 | |
| 反應前:燒杯+鹽酸 | 22g |
| 10片鈣片 | 8g |
| 反應后:燒杯+剩余物 | 27.8g |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com