
分析 (一)(1)根據鐵和硫酸銅反應生成硫酸亞鐵和銅進行分析;
(2)根據材料的分類解答;
(3)根據胃酸的主要成分是鹽酸,鹽酸和鐵反應會生成氯化亞鐵和氫氣進行分析;
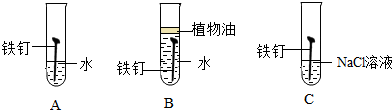
(二)(1)根據鐵生銹的條件進行解答;
(2)根據鐵與水和氧氣作用下生成氫氧化亞鐵進行分析;
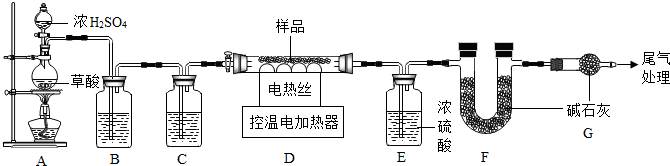
(3)①根據有氣體參加或生成的反應,組裝好儀器后,要先檢驗裝置氣密性,再裝藥品進行反應;
②根據草酸分解生成水、二氧化碳、一氧化碳,在一氧化碳參與反應之前,需要先將二氧化碳和水除去進行分析;
③根據濃硫酸有吸水性,堿石灰會與二氧化碳反應進行分析;
④根據空氣中的二氧化碳、水會與堿石灰反應進行分析;
(三)(1)根據一氧化碳和氧化鐵在高溫的條件下反應生成鐵和二氧化碳進行分析;
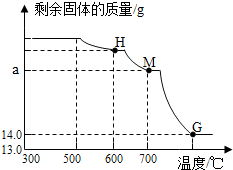
(2)根據碳酸亞鐵分解生成氧化亞鐵和二氧化碳,一氧化碳還原氧化鐵的三個階段的反應可知,M點實際是一氧化碳將氧化鐵還原生成了氧化鐵和碳酸亞鐵分解生成氧化亞鐵的質量之和,結合前面計算出的碳酸亞鐵的質量、氧化鐵的質量即可求出M點的數值.
解答 解:(一)(1)硫酸銅溶液遇到金屬鐵時,鐵與硫酸銅發生置換反應能生成金屬銅,化學方程式為:Fe+CuSO4=Cu+FeSO4;
(2)不銹鋼絲屬于金屬材料,聚乙烯纖維屬于合成材料,耐酸防護服材料屬于復合材料,故選:B;
(3)胃酸的主要成分是鹽酸,鹽酸和鐵反應會生成氯化亞鐵和氫氣,化學方程式為:Fe+2HCl═FeCl2+H2↑;
(二)(1)鐵生銹時,需要水分和氧氣同時存在,當有鹽類物質存在時,生銹速度加快,故選:C;
(2)鐵與水和氧氣作用下生成氫氧化亞鐵,化學方程式為:2Fe+O2+2H2O═2Fe(OH)2;
(3)①有氣體參加或生成的反應,組裝好儀器后,要先檢驗裝置氣密性,再裝藥品進行反應;
②依據質量守恒定律可知,生成物中有氫元素,所以反應物中也必須有氫元素,草酸分解生成水、二氧化碳、一氧化碳,在一氧化碳參與反應之前,需要先將二氧化碳和水除去,濃硫酸有吸水性,氫氧化鈉會與二氧化碳反應,要先除二氧化碳,在除水蒸氣,所以洗氣瓶B中應盛放氫氧化鈉溶液,故選:c;
③濃硫酸有吸水性,堿石灰會與二氧化碳反應,加熱到了300℃,所以一氧化碳不會還原氧化鐵,濃硫酸增加的質量是水的質量,來自鐵銹,堿石灰增加的質量來自碳酸亞鐵分解生成的二氧化碳,所以依據元素守恒進行計算
設碳酸亞鐵的質量為y,
$\frac{12}{116}$×y=$\frac{12}{44}$×2.2g
y=5.8g
所以Fe2O3•xH2O為:25.4g-5.8g=19.6g,氧化鐵的質量為:$\frac{160}{196}$×19.6g=16g
$\frac{2x}{160+18x}$×19.6g=$\frac{2}{18}$×3.6g
x=2;
④空氣中的二氧化碳、水會與堿石灰反應,導致F裝置中收集的二氧化碳質量偏大,所以碳酸亞鐵質量偏大,Fe2O3•xH2O,所以x質量偏大;
(三)(1)一氧化碳和氧化鐵在高溫的條件下反應生成鐵和二氧化碳,化學方程式為:Fe2O3+3CO$\frac{\underline{\;高溫\;}}{\;}$2Fe+3CO2;
(2)設碳酸亞鐵生成的氧化亞鐵質量為a,
FeCO3→FeO
116 72
5.8g a
$\frac{116}{5.8g}$=$\frac{72}{a}$
a=3.6g
氧化鐵生成的氧化亞鐵質量為b,
Fe2O3→2FeO
160 144
16g b
$\frac{160}{16g}$=$\frac{144}{b}$
b=14.4g
所以M=14.4g+3.6g=18g.
故答案為:
(一)(1)Fe+CuSO4=FeSO4+Cu;
(2)B;
(3)Fe+2HCl═FeCl2+H2↑;
(二)(1)C;
(2)2Fe+O2+2H2O═2Fe(OH)2;
(三)(1)檢查裝置的氣密性;
(2)H,c;
(3)5.8,2;
(4)偏大,偏大;
(三)(1)Fe2O3+3CO$\frac{\underline{\;高溫\;}}{\;}$2Fe+3CO2;
(2)18.
點評 本題考查一氧化碳還原鐵的氧化物的步驟、現象、化學反應式的書寫,以及用不同的方法驗證鐵的存在,需要同學們具有比較全面的化學知識.


科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 0.1g | B. | 0.2g | C. | 0.3g | D. | 0.4g |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
 為驗證混合氣體中是否含有CO,CO2,H2O,H2 這四種氣體,現有無水硫酸銅,澄清石灰水,濃硫酸,氫氧化鈉溶液以及如圖所示裝置甲.能驗證這四種氣體的方法正確的是( )
為驗證混合氣體中是否含有CO,CO2,H2O,H2 這四種氣體,現有無水硫酸銅,澄清石灰水,濃硫酸,氫氧化鈉溶液以及如圖所示裝置甲.能驗證這四種氣體的方法正確的是( )| A. | 依次通入無水硫酸銅,澄清石灰水,濃硫酸,甲裝置,無水硫酸銅,澄清石灰水 | |
| B. | 依次通入無水硫酸銅,澄清石灰水,甲裝置,無水硫酸銅,澄清石灰水 | |
| C. | 依次通入澄清石灰水,無水硫酸銅,濃硫酸,甲裝置,無水硫酸銅,澄清石灰水 | |
| D. | 依次通入無水硫酸銅,澄清石灰水,濃硫酸,甲裝置,澄清石灰水,無水硫酸銅 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
 元素周期表是學習化學的重要工具.如表是元素周期表的一部分,請依據此表回答有關問題.
元素周期表是學習化學的重要工具.如表是元素周期表的一部分,請依據此表回答有關問題.| 第一周期 | 1 H 1.008 | 2 He 4.003 | ||||||
| 第二周期 | 3 Li 6.941 | 4 Be 9.012 | 5 B 10.81 | 6 C 12.01 | 7 N 14.01 | 8 O 16.00 | 9 F 19.00 | 10 Ne 20.18 |
| 第三周期 | 11 Na 22.99 | 12 Mg 24.31 | 13 Al 26.98 | 14 Si 28.09 | 15 P 30.97 | 16 S 32.06 | 17 Cl 35.45 | 18 Ar 39.95 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com