
科目: 來源: 題型:
【題目】下列敘述中正確的是( )
A. 能電離出H+的化合物除水外都是酸,分子中含有幾個氫原子它就是幾元酸
B. 無機含氧酸分子中含有幾個羥基,它就屬于幾元酸
C. 同一元素的含氧酸,該元素的化合價越高,其酸性越強,氧化性也越強
D. H3PO4和H2CO3分子中非羥基氧的個數均為1,但它們的酸性不相近,H3PO4是中強酸而H2CO3是弱酸
查看答案和解析>>
科目: 來源: 題型:
【題目】油脂是重要的營養物質.某天然油脂A可發生下列反應:

已知:A的分子式為C57H106O6.1mol該天然油脂A經反應①可得到1molD、1mol不飽和脂肪酸B和2mol直鏈飽和脂肪酸C.經測定B的相對分子質量為280,原子個數比為C:H:O=9:16:1;
(1)寫出B的分子式:________________________;
(2)寫出反應①的反應類型:____________;C的名稱(或俗稱)是_________;
(3)近日,電視媒體關于“氫化油危害堪比殺蟲劑”的報道引發軒然大波,反應②為天然油脂的氫化過程.下列有關說法不正確的是_______________;
a.氫化油又稱人造奶油,通常又叫硬化油.
b.植物油經過氫化處理后會產生副產品反式脂肪酸甘油酯,攝入過多的氫化油,容易堵塞血管而導致心腦血管疾病.
c.氫化油的制備原理是在加熱植物油時,加入金屬催化劑,通入氫氣,使液態油脂變為半固態或固態油脂.
d.油脂的氫化與油脂的皂化都屬于加成反應
(4)D和足量金屬鈉反應的化學方程式_____________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】某溫度下,在2L的密閉容器中,X、Y、Z三種物質隨時間變化的曲線如圖所示.請回答下列問題
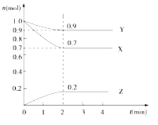
(1)由圖中數據分析,該反應的化學方程式為___________________________
(2)反應開始至2min,Z的平均反應速率為________
(3)3min時,Z的生成速率與Z的消耗速率相比較,前者________(填“大于”“小于”或“等于”)后者.
(4)上述反應進行過程中,如果降低溫度,則其反應速率________(填“增大”“減小”或“不變”).
(5)下列各項中不可以說明上述反應達到平衡的是________(填字母).
a.生成1molZ和同時生成1.5molX b. X、Y、Z的反應速率之比為3:2:1
c.同一物質的正反應速率等于逆反應速率 d.X的濃度保持不變
查看答案和解析>>
科目: 來源: 題型:
【題目】鉛蓄電池反應原理為:Pb(s)+PbO2(s)+2H2SO4(aq)![]() 2PbSO4(s)+2H2O(l),下列說法正確的是
2PbSO4(s)+2H2O(l),下列說法正確的是
A.放電時,正極附近pH 減小
B.充電時,鉛蓄電池的負極連接電源的正極
C.放電時,負極的電極反應式為:Pb-2e-=Pb2+
D.充電時,陰極的電極反應式為:PbSO4+2e-=Pb+![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】利用如圖裝置來驗證同主族元素非金屬性的變化規律。
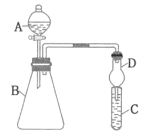
要證明非金屬性:Cl>I,在A中加入濃鹽酸,B中加入KMnO4(KMnO4與濃鹽酸在常溫下反應生成氯氣),C中加入___溶液,觀察到C中___(填實驗現象),即可證明。干燥管D的作用是___。從環境保護的角度考慮,此裝置尚缺少尾氣處理裝置,可用___溶液吸收尾氣。
查看答案和解析>>
科目: 來源: 題型:
【題目】溫度容積相同的3個密閉容器中,按不同方式投入反應物并保持恒溫恒容,測得反應達到平衡時的有關數據如下![]() 已知:
已知:![]()
容器 | 甲 | 乙 | 丙 |
反應物投入量 | 1mol | 2mol | 4mol |
|
|
|
|
反應的能量變化 | 放出akJ | 吸收bkJ | 吸收ckJ |
體系壓強 |
|
|
|
反應物轉化率 |
|
|
|
下列說法正確的是
A.![]() B.
B.![]() C.2
C.2![]() D.
D.![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】在 2L 密閉容器中,3mol A 和 1molB 發生反應:3A(g)+B(g)2C(g)+2D(g),10s 末時,生成 1.2mol C,下列說法正確的是
A.10s 內,v(D)=0.12 mol/(L·s)B.10s 末時,物質 A 的轉化率為 60%
C.10s 末時,B的濃度為0.3mol/LD.10s 末時,C 的物質的量分數為 15%
查看答案和解析>>
科目: 來源: 題型:
【題目】把3.0mol M和2.5mol N混合于2.0L的恒容密閉容器中,發生反應3M(g) + N(g)![]() xP(g) +2Q(g),5min反應達到平衡,已知M的轉化率為50%,P的反應速率為0.15mol·L-1·min-1,則下列說法正確的是()
xP(g) +2Q(g),5min反應達到平衡,已知M的轉化率為50%,P的反應速率為0.15mol·L-1·min-1,則下列說法正確的是()
A.方程式中x=2
B.達平衡后,容器內壓強是反應起始時的2倍
C.向容器中再充入3.0molM和2.5molN,達新平衡時Q的體積分數減小
D.容器內混合氣體的密度不再變化和平均相對分子質量不再變化均可作為達到平衡狀態的標志
查看答案和解析>>
科目: 來源: 題型:
【題目】解釋下列過程的離子方程式不正確的是
A.K2Cr2O7 溶液中加入濃 NaOH 溶液后變黃:![]() +H2O
+H2O![]() 2
2![]() +2H+
+2H+
B.明礬溶于水產生Al(OH)3 膠體:Al3++3H2O![]() Al(OH)3(膠體)+3H+
Al(OH)3(膠體)+3H+
C.用碳酸鈉溶液處理鍋爐水垢中的硫酸鈣:CaSO4+![]() ==CaCO3+
==CaCO3+![]()
D.向Ca(HCO3)2 溶液中滴加少量 NaOH 溶液生成白色沉淀:Ca2++2![]() +2OH-=CaCO3↓+
+2OH-=CaCO3↓+![]() +2H2O
+2H2O
查看答案和解析>>
科目: 來源: 題型:
【題目】焦炭催化還原二氧化硫的化學方程式為2C(s)+2SO2(g) ![]() S2(g)+2CO2(g)。一定壓強下,向1L密閉容器中充入足量的焦炭和1molSO2發生反應,測得SO2的生成速率與S2(g)的生成速率隨溫度變化的關系如圖所示,下列說法正確的是
S2(g)+2CO2(g)。一定壓強下,向1L密閉容器中充入足量的焦炭和1molSO2發生反應,測得SO2的生成速率與S2(g)的生成速率隨溫度變化的關系如圖所示,下列說法正確的是
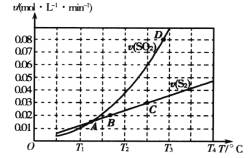
A. 該反應的H>0B. C點時達到平衡狀態
C. 增加C的量能夠增大SO2的轉化率D. T3時增大壓強,能增大活化分子百分數
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com