
科目: 來源: 題型:
【題目】硫代硫酸鈉(Na2S2O3)是一種解毒藥,用于氟化物、砷、汞、鉛、錫、碘等中毒,臨床常用于治療蕁麻疹,皮膚瘙癢等病癥.硫代硫酸鈉在中性或堿性環境中穩定,在酸性溶液中分解產生S和SO2
實驗I:Na2S2O3的制備。工業上可用反應:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,實驗室模擬該工業過程的裝置如圖所示:

(1)儀器a的名稱是_______,儀器b的名稱是_______。b中利用質量分數為70%80%的H2SO4溶液與Na2SO3固體反應制備SO2反應的化學方程式為_______。c中試劑為_______
(2)實驗中要控制SO2的生成速率,可以采取的措施有_______ (寫出一條)
(3)為了保證硫代硫酸鈉的產量,實驗中通入的SO2不能過量,原因是_______
實驗Ⅱ:探究Na2S2O3與金屬陽離子的氧化還原反應。
資料:Fe3++3S2O32-Fe(S2O3)33-(紫黑色)
裝置 | 試劑X | 實驗現象 |
| Fe2(SO4)3溶液 | 混合后溶液先變成紫黑色,30s后幾乎變為無色 |
(4)根據上述實驗現象,初步判斷最終Fe3+被S2O32-還原為Fe2+,通過_______(填操作、試劑和現象),進一步證實生成了Fe2+。從化學反應速率和平衡的角度解釋實驗Ⅱ的現象:_______
實驗Ⅲ:標定Na2S2O3溶液的濃度
(5)稱取一定質量的產品配制成硫代硫酸鈉溶液,并用間接碘量法標定該溶液的濃度:用分析天平準確稱取基準物質K2Cr2O7(摩爾質量為294gmol-1)0.5880g。平均分成3份,分別放入3個錐形瓶中,加水配成溶液,并加入過量的KI并酸化,發生下列反應:6I-+Cr2O72-+14H+ = 3I2+2Cr3++7H2O,再加入幾滴淀粉溶液,立即用所配Na2S2O3溶液滴定,發生反應I2+2S2O32- = 2I- + S4O62-,三次消耗 Na2S2O3溶液的平均體積為25.00 mL,則所標定的硫代硫酸鈉溶液的濃度為_______molL-1
查看答案和解析>>
科目: 來源: 題型:
【題目】節日期間因燃放鞭炮會引起空氣中SO2含量增高,造成大氣污染。某實驗小組同學欲探究SO2的性質,并測定空氣中SO2的含量。
(1)他們設計如下實驗裝置,請你參與探究,并回答問題:
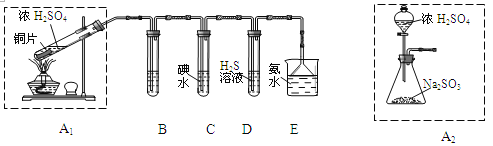
①裝置A1中發生反應的化學方程式為 ;
②裝置B用于檢驗SO2的漂白性,其中所盛試劑為 ,裝置D用于檢驗SO2的 性質;
③裝置C中反應的離子方程式為 ;
④為了實現綠色環保的目標,甲同學欲用裝置A2代替裝置A1,你認為裝置A2的優點是(寫二點) 、 ;
(2)他們擬用以下方法測定空氣中SO2含量(假設空氣中無其他還原性氣體)。
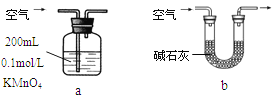
①你認為哪個裝置可行(填序號) ,使用你所選用的裝置測定SO2含量時,還需要測定的物理量是 ;
②你認為哪個裝置不可行(填序號) ,說明理由 。
查看答案和解析>>
科目: 來源: 題型:
【題目】25℃時,某溶液中由水電離出的c(OH-)=1×10-13mol/L,該溶液中一定不能大量共存的離子組是( )
A.NH![]() 、Fe3+、SO
、Fe3+、SO![]() 、Cl-B.CO
、Cl-B.CO![]() 、PO
、PO![]() 、K+、Na+
、K+、Na+
C.Na+、SO![]() 、NO
、NO![]() 、Cl-D.HPO
、Cl-D.HPO![]() 、Na+、HSO
、Na+、HSO![]() 、K+
、K+
查看答案和解析>>
科目: 來源: 題型:
【題目】已知 A、B、C、D、E 五種主族元素分屬三個短周期,且原子序數依次增大。A、C 同主族,可形成離子化合物 CA;B、D 同主族,可形成 DB2、DB3 兩種分子。請回答下列問題:
(1)五種元素原子半徑由小到大的順序為_______________(用元素符號回答)。
(2)A、B 兩種元素能形成既含極性鍵又含非極性鍵的化合物 M,M 的電子式為_______________。
(3)非金屬性強弱:D_______________E(填“>”“<”),用離子方程式表示__________________________。
(4)寫出均由 A、B、C、D 四種元素組成的兩物質的濃溶液發生反應的離子方程式_____________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】影響化學反應速率的因素很多,某化學小組用實驗的方法進行探究。
Ⅰ.探究一:備選藥品:鎂片、鋁片、0.500 mol·L-1H2SO4、18.4 mol·L-1H2SO4。
甲同學研究的實驗報告:
實驗步驟 | 現象 | 結論 |
①用砂紙打磨鎂片和鋁片; ②分別取等體積等濃度的硫酸于兩支試管中; ③將鎂片和鋁片同時投入到試管中。 | 金屬的性質越活潑, 反應速率越快 |
(1)甲同學用砂紙打磨鎂片和鋁片的原因是______________________________;選擇H2SO4濃度為________________。
(2) 實驗報告中現象為_______________________________________________。
Ⅱ.探究二:實驗室經常用Na2S2O3與H2SO4的反應探究化學反應速率的影響因素,利用圖1所示裝置(夾持裝置略去)進行實驗,觀察到錐形瓶底部有淡黃色渾濁。
(3)請用化學方程式表示出實驗原理_________________________________,乙同學在實驗過程中對產生的氣體進行收集,并在2min內6個時間點對注射器內氣體進行讀數,記錄數據并繪制出圖像(如圖2)。
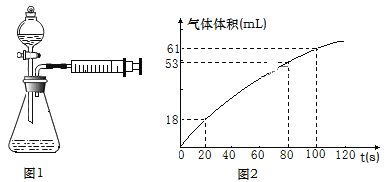
0~20s內反應速率υ1=__________mL·s-1,80~100s內反應速率υ2=__________mL·s-1。不考慮實驗測量誤差,分析速率差異的主要原因是_____________。
查看答案和解析>>
科目: 來源: 題型:
【題目】在容積不變的密閉容器中存在如下反應:![]()
![]() 。在其他條件不變時,只改變某一個條件,可得到下列圖像:
。在其他條件不變時,只改變某一個條件,可得到下列圖像:
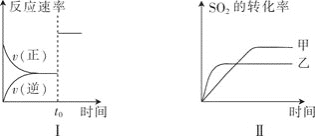
則下列有關敘述中正確的是![]()
![]()
A.圖Ⅰ可以表示![]() 時刻增大
時刻增大![]() 的濃度
的濃度
B.圖Ⅰ可以表示![]() 時刻加入催化劑
時刻加入催化劑
C.圖Ⅱ可以表示兩種不同壓強下![]() 的轉化率與時間的關系,且乙的壓強比甲高
的轉化率與時間的關系,且乙的壓強比甲高
D.圖Ⅱ可以表示兩種不同溫度下![]() 的轉化率與時間的關系,且甲的溫度比乙高
的轉化率與時間的關系,且甲的溫度比乙高
查看答案和解析>>
科目: 來源: 題型:
【題目】A、B、C、D、E、F、G、H 是元素周期表前四周期常見元素,且原子序數依次增大,其相關信息如下表:
元素 | 相關信息 |
A | 原子核外有 6 種不同運動狀態的電子 |
C | 基態原子中 s 電子總數與p 電子總數相等 |
D | 原子半徑在同周期元素中最大 |
E | 基態原子最外層電子排布式為 3s23p1 |
F | 基態原子的最外層 p 軌道有兩個電子的自旋方向與其他電子的自 旋方向相反 |
G | 基態原子核外有 7 個能級且能量最高的能級上有 6 個電子 |
H | 是我國使用最早的合金中的最主要金屬元素 |
(1) A 元素的名稱是_______________;A 元素和 F 元素形成的最簡單化合物的分子構型為_______________,該分子是_______________分子。(填“極性”或“非極性”)
(2) B 元素形成的單質分子中σ鍵與π鍵數目之比為_______________。
(3) G 元素的低價陽離子的離子結構示意圖是_______________。
(4) G 的高價陽離子的溶液與 H 單質反應的離子方程式為___________________________________
查看答案和解析>>
科目: 來源: 題型:
【題目】一定溫度下,在三個體積均為0.5 L的恒容密閉容器中發生反應:CO(g)+Cl2(g) ![]() COCl2(g),其中容器Ⅰ中反應在5 min時達到平衡狀態。
COCl2(g),其中容器Ⅰ中反應在5 min時達到平衡狀態。
容器編號 | 溫度/℃ | 起始物質的量/mol | 平衡物質的量/mol | ||
CO | Cl2 | COCl2 | COCl2 | ||
Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
Ⅱ | 500 | 1.0 | a | 0 | 0.5 |
Ⅲ | 600 | 0.5 | 0.5 | 0.5 | 0.7 |
下列說法中正確的是
A.該反應正反應為放熱反應
B.容器Ⅰ中前5 min的平均反應速率υ(CO)=0.16 mol·L-1·min-1
C.容器Ⅱ中,a=0.55 mol
D.若容器Ⅰ為恒壓,達到平衡時CO轉化率小于80%
查看答案和解析>>
科目: 來源: 題型:
【題目】(1)某元素的全部電離能(單位:eV)如下:
I1 | I2 | I3 | I4 | I5 | I6 | I7 | I8 |
13.6 | 35.1 | 54.9 | 77.4 | 113.9 | 138.1 | 739.1 | 871.1 |
寫出該元素價電子軌道表示式_______________。
(2)分子中的大π 鍵可用符號![]() 表示,其中 m 代表參與形成大 π 鍵的原子數,n 代表參與形成大π 鍵的電子數,如苯分子中的大 π 鍵可表示為
表示,其中 m 代表參與形成大 π 鍵的原子數,n 代表參與形成大π 鍵的電子數,如苯分子中的大 π 鍵可表示為![]() 。
。
①試判斷 SO2 最外層一共有_______________對孤對電子。
②HN3稱為疊氮酸,常溫下為無色有刺激性氣味的液體。N3-的鍵角為_______________,N![]() 中的大π 鍵應表示為_______________。
中的大π 鍵應表示為_______________。
(3)根據對角線規則,Be、Al 的化學性質相似,寫出 Be(OH)2 與 NaOH 反應的離子方程式是________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com