
科目: 來源: 題型:
【題目】有機物的結構可用“鍵線式”表示,如:CH3CHCHCH3可簡寫為![]() 。有機物X的鍵線式為
。有機物X的鍵線式為![]() ,下列說法不正確的是( )
,下列說法不正確的是( )
A.X的化學式為C8H8
B.有機物Y是X的同分異構體,且屬于芳香烴,則Y的結構簡式為![]()
C.X能使酸性高錳酸鉀溶液褪色
D.X與足量的H2在一定條件下反應可生成環狀的飽和烴Z,Z的一氯代物有4種
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖是Zn和Cu組成的原電池示意圖,某小組做完該實驗后,在讀書卡片上記錄如下,卡片上描述合理的是( )
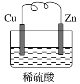
實驗記錄:
①導線中電流方向:Zn→Cu
②Cu極上有氣泡產生,發生還原反應
③鋅片變薄
實驗結論:
④Zn為正極,Cu為負極
⑤正極反應式:Cu-2e-=Cu2+,發生氧化反應
⑥H+向Cu極移動,SO42-向Zn極移動
A.②③⑥B.④⑤⑥
C.③④⑤D.①②③
查看答案和解析>>
科目: 來源: 題型:
【題目】實驗室以工業廢渣(主要含CaSO4·2H2O,還含少量SiO2、Al2O3、Fe2O3)為原料制取輕質CaCO3和(NH4)2SO4晶體,其實驗流程如下:
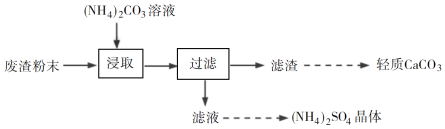
(1)室溫下,反應CaSO4(s)+![]() (aq)
(aq)![]() CaCO3(s)+
CaCO3(s)+![]() (aq)達到平衡,則溶液中
(aq)達到平衡,則溶液中 =________[Ksp(CaSO4)=4.8×105,Ksp(CaCO3)=3×109]。
=________[Ksp(CaSO4)=4.8×105,Ksp(CaCO3)=3×109]。
(2)將氨水和NH4HCO3溶液混合,可制得(NH4)2CO3溶液,其離子方程式為________;浸取廢渣時,向(NH4)2CO3溶液中加入適量濃氨水的目的是________。
(3)廢渣浸取在如圖所示的裝置中進行。控制反應溫度在60~70 ℃,攪拌,反應3小時。溫度過高將會導致CaSO4的轉化率下降,其原因是________;保持溫度、反應時間、反應物和溶劑的量不變,實驗中提高CaSO4轉化率的操作有________。

(4)濾渣水洗后,經多步處理得到制備輕質CaCO3所需的CaCl2溶液。設計以水洗后的濾渣為原料,制取CaCl2溶液的實驗方案:______[已知pH=5時Fe(OH)3和Al(OH)3沉淀完全;pH=8.5時Al(OH)3開始溶解。實驗中必須使用的試劑:鹽酸和Ca(OH)2]。
查看答案和解析>>
科目: 來源: 題型:
【題目】鐵、鎳及其化合物在工業上有廣泛的應用。從某礦渣 ![]() 成分為
成分為![]() 鐵酸鎳
鐵酸鎳![]() 、NiO、FeO、CaO、
、NiO、FeO、CaO、![]() 等
等![]() 中回收
中回收![]() 的工藝流程如下:
的工藝流程如下:
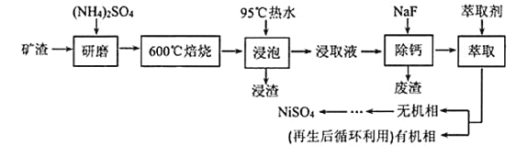
已知![]() 在
在![]() 分解生成
分解生成![]() 和
和![]() ,回答下列問題:
,回答下列問題:
![]() “浸渣”的成分有
“浸渣”的成分有![]() 、
、![]() 、
、![]() 外,還含有_________
外,還含有_________![]() 寫化學式
寫化學式![]() 。
。
![]() 礦渣中部分FeO焙燒時與
礦渣中部分FeO焙燒時與![]() 反應生成
反應生成![]() 的化學方程式為_____________。
的化學方程式為_____________。
![]() 溶劑萃取可用于對溶液中的金屬離子進行富集與分離:
溶劑萃取可用于對溶液中的金屬離子進行富集與分離:![]() 水相
水相![]() 有機相
有機相![]() 有機相
有機相![]() 水相
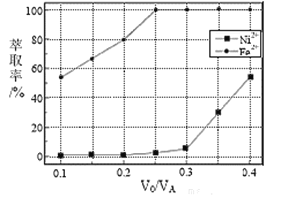
水相![]() 。萃取劑與溶液的體積比
。萃取劑與溶液的體積比![]() 對溶液中
對溶液中![]() 、
、![]() 的萃取率影響如下圖所示,
的萃取率影響如下圖所示,![]() 的最佳取值為________。在_______
的最佳取值為________。在_______![]() 填“強堿性”“強酸性”或“中性”
填“強堿性”“強酸性”或“中性”![]() 介質中“反萃取”能使有機相再生而循環利用。
介質中“反萃取”能使有機相再生而循環利用。
![]() 以Fe、Ni為電極制取
以Fe、Ni為電極制取![]() 的原理如下圖所示。通電后,在鐵電極附近生成紫紅色的
的原理如下圖所示。通電后,在鐵電極附近生成紫紅色的![]() ,若pH過高,鐵電極區會產生紅褐色物質。
,若pH過高,鐵電極區會產生紅褐色物質。
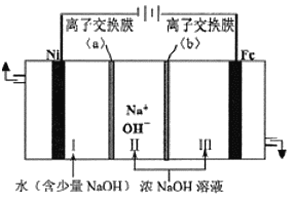
![]() 電解時陽極的電極反應式為_________,離子交換膜
電解時陽極的電極反應式為_________,離子交換膜![]() 為________
為________![]() 填“陰”或“陽
填“陰”或“陽![]() 離子交換膜。
離子交換膜。
![]() 向鐵電極區出現的紅褐色物質中加入少量的NaClO溶液,沉淀溶解。該反應的離子方程式為__________。
向鐵電極區出現的紅褐色物質中加入少量的NaClO溶液,沉淀溶解。該反應的離子方程式為__________。
查看答案和解析>>
科目: 來源: 題型:
【題目】可逆反應2NO2![]() 2NO+O2在密閉容器中反應,達到平衡狀態的標志是( )
2NO+O2在密閉容器中反應,達到平衡狀態的標志是( )
①單位時間內生成nmolO2的同時生成2nmolNO2
②單位時間內生成nmolO2的同時生成2nmolNO
③用NO2、NO、O2的物質的量濃度變化表示的反應速率的比為2∶2∶1的狀態
④混合氣體的顏色不再改變的狀態
A.②③B.①④
C.①③④D.①②③④
查看答案和解析>>
科目: 來源: 題型:
【題目】影響化學反應速率的因素很多,某課外興趣小組用實驗的方法進行探究。
(1)實驗一:取等物質的量濃度等體積H2O2溶液分別進行下列實驗,實驗報告如下表所示。

試回答:
①實驗1、2研究的是__________________________對H2O2分解速率的影響。
②實驗2、3的目的是_______________________________________________。
(2)實驗二:經研究知Cu2+對H2O2分解也具有催化作用,為比較Fe3+和Cu2+對H2O2分解的催化效果,該小組的同學分別設計了如圖甲、乙所示的實驗。回答相關問題:

① 定性分析:如圖甲可通過觀察________________________________,定性比較得出結論。有同學提出將FeCl3改為Fe2(SO4)3更為合理,其理由是_________________________。
②定量分析:如圖乙所示,實驗時均以生成40 mL氣體為準,其他可能影響實驗的因素均已忽略。實驗中需要測量的數據是__________________________________。
(3)實驗三:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高錳酸鉀酸性溶液和草酸溶液反應時,發現開始一段時間,反應速率較慢,溶液褪色不明顯但不久突然褪色,反應速率明顯加快。
①針對上述實驗現象,某同學認為KMnO4與H2C2O4反應是放熱反應,導致溶液溫度升高,反應速率加快。從影響化學反應速率的因素看,你的猜想還可能是_____________________的影響。
②若用實驗證明你的猜想,除酸性高錳酸鉀溶液、草酸溶液試劑外,還需要選擇的試劑最合理的是_________。
A、硫酸鉀 B、硫酸錳 C、水 D、氯化錳
查看答案和解析>>
科目: 來源: 題型:
【題目】![]() 以
以![]() 和
和![]() 為原料合成尿素是利用
為原料合成尿素是利用![]() 的成功范例。在尿素合成塔中的主要反應可表示如下:
的成功范例。在尿素合成塔中的主要反應可表示如下:
反應Ⅰ:![]()
![]()
反應Ⅱ:![]()
![]()
總反應:![]()
![]()
請回答下列問題:
![]() 反應Ⅰ的
反應Ⅰ的![]() ______________。
______________。
![]() 在____
在____![]() 填“高溫”或“低溫”
填“高溫”或“低溫”![]() 情況下有利于反應Ⅱ的自發進行。
情況下有利于反應Ⅱ的自發進行。
![]() 氨法溶浸氧化鋅煙灰制取高純鋅的工藝流程如圖所示。溶浸后氧化鋅煙灰中鋅、銅、鎘、砷元素分別以
氨法溶浸氧化鋅煙灰制取高純鋅的工藝流程如圖所示。溶浸后氧化鋅煙灰中鋅、銅、鎘、砷元素分別以![]() 、
、![]() 、
、![]() 、
、![]() 的形式存在。
的形式存在。

![]() “溶浸”中 ZnO發生反應的離子方程式為 _______。
“溶浸”中 ZnO發生反應的離子方程式為 _______。
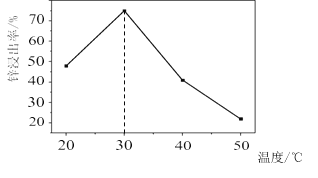
![]() 鋅浸出率與溫度的關系如圖所示,分析
鋅浸出率與溫度的關系如圖所示,分析 ![]() 時鋅浸出率最高的原因為 __________。
時鋅浸出率最高的原因為 __________。
![]() “濾渣 3”的主要成分為_______________。
“濾渣 3”的主要成分為_______________。
查看答案和解析>>
科目: 來源: 題型:
【題目】北京冬奧會將于2022年舉辦,節儉辦賽是主要理念。在場館建設中用到一種耐腐、耐高溫的表面涂料是以某雙環烯酯為原料制得,該雙環烯酯的結構如圖所示(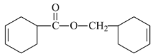 )。下列說法正確的是
)。下列說法正確的是
A.該雙環烯酯的水解產物都能使溴水褪色
B.1 mol該雙環烯酯能與3 mol H2發生加成反應
C.該雙環烯酯分子中至少有12個原子共平面
D.該雙環烯酯完全加氫后的產物的一氯代物有7種
查看答案和解析>>
科目: 來源: 題型:
【題目】對可逆反應4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列敘述正確的是( )
4NO(g)+6H2O(g),下列敘述正確的是( )
A. 達到化學平衡時4v正(O2)=5v逆(NO)
B. 若單位時間內生成x mol NO的同時,消耗x mol NH3,則反應達到平衡狀態
C. 達到化學平衡時,若增大容器容積,則正反應速率減小,逆反應速率增大
D. 化學反應速率關系:2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目: 來源: 題型:
【題目】化學與生活、社會發展息息相關,下列有關說法不正確的是
A.尼龍屬于有機高分子材料
B.稻草秸稈和甘蔗渣中富含纖維素,可以用它來制造紙張
C.將大橋鋼制構件用導線與石墨相連可以起到防腐的作用
D.劉禹錫![]() 浪淘沙
浪淘沙![]() 詩句“千淘萬漉雖辛苦,吹盡黃沙始到金”中“淘”“漉”相當于“過濾”
詩句“千淘萬漉雖辛苦,吹盡黃沙始到金”中“淘”“漉”相當于“過濾”
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com