
科目: 來源: 題型:選擇題
| A. | 油脂、乙酸乙酯都屬于酯類,水解后都會生成乙醇 | |
| B. | 人的皮膚在強紫外線的照射下將會失去生理活性 | |
| C. | 棉花和蠶絲的主要成分都是纖維素 | |
| D. | 制作航天服的聚酯纖維和用于光纜通信的光導纖維都是新型無機非金屬材料 |
查看答案和解析>>
科目: 來源: 題型:解答題
| 物質 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 開始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |

查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | ①③⑤⑦ | B. | ③④⑤⑥ | C. | ①②⑤⑦ | D. | ①②⑥⑦ |
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. |  ? ?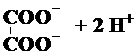 | B. | Ba(OH)2?Ba2++2OH- | ||
| C. | HCO3-+H2O?H3O++CO32- | D. | NaHCO3═Na++H++CO32- |
查看答案和解析>>
科目: 來源: 題型:解答題
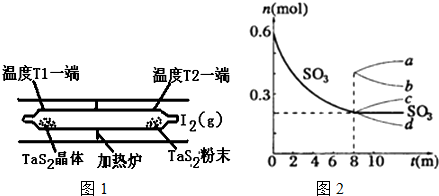
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 用水稀釋0.1 mol/L的氨水,則溶液中$\frac{c(C{H}_{3}.{H}_{2}O)}{c(O{H}^{-})}$增大 | |
| B. | 在等體積等pH 的鹽酸和醋酸兩溶液中分別加入等質量的相同鋅粒,若只有一種溶液中的鋅粒有剩余,則該溶液一定是鹽酸 | |
| C. | pH=3的鹽酸和醋酸分別升高相同的溫度,pH均不變 | |
| D. | 兩種氨水溶液的物質的量濃度分別為C1和C2,pH分別為a和a+1,則C2=10C1 |
查看答案和解析>>
科目: 來源: 題型:解答題
| 溫度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡總壓強(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡氣體總濃度 | |||||
| (×10-3 mol•L-1) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com