
科目: 來源: 題型:解答題
 +
+ $?_{△}^{濃H_{2}SO_{4}}$
$?_{△}^{濃H_{2}SO_{4}}$ +H2O
+H2O| 相對分子質量 | 密度/(g•cm-3) | 沸點/℃ | 水中溶解性 | |
| 異戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸異戊酯 | 130 | 0.8670 | 142 | 難溶 |

查看答案和解析>>
科目: 來源: 題型:解答題

| 溶液中被沉淀離子 | Fe3+ | Fe2+ | Cu2+ |
| 完全生成氫氧化物沉淀時,溶液的pH | ≥3.7 | ≥6.4 | ≥4.4 |
查看答案和解析>>
科目: 來源: 題型:解答題

 $\stackrel{過氧化物}{→}$
$\stackrel{過氧化物}{→}$ (R,R′代表烴基)
(R,R′代表烴基) .
. .
.查看答案和解析>>
科目: 來源: 題型:解答題
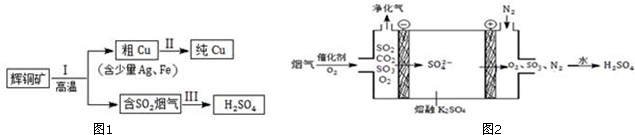
查看答案和解析>>
科目: 來源: 題型:解答題
 氯元素是生產生活中常見的非金屬元素
氯元素是生產生活中常見的非金屬元素查看答案和解析>>
科目: 來源: 題型:解答題

查看答案和解析>>
科目: 來源: 題型:解答題
 已知25℃時部分弱電解質的電離平衡常數數據如表所示:
已知25℃時部分弱電解質的電離平衡常數數據如表所示:| 化學式 | CH3COOH | H2CO3 | HClO | |
| 電離平衡常數 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
查看答案和解析>>
科目: 來源: 題型:解答題

查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 18 g H2O含有10NA個質子 | |
| B. | 1 mol/LCH3COONa溶液中含有1 mol/LCH3COO- | |
| C. | 標準狀況下,22.4 L氨水含有NA個NH3分子 | |
| D. | 56 g鐵片投入足量濃H2SO4中生成NA個SO2分子 |
查看答案和解析>>
科目: 來源: 題型:解答題

 .
.
 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com