

 .
.
 .
. 分析 Ⅰ、由龍膽酸甲酯的結構可知,分子中含有酚羥基,具有酚的性質,酚羥基的酸性小于碳酸,與碳酸鈉反應生成碳酸氫鈉,含有酯基,具有酯的性質,含有苯環,可以發生加成反應,據此結合選項解答;
Ⅱ、X在稀硫酸、加熱條件下生成龍膽酸與A,為酯的水解反應,A為醇,A發生消去反應生成C4H8,A與B互為同分異構體,B能催化氧化生成C,C能發生銀鏡反應,故B中-OH連接的碳原子上含有2個H原子,B為(CH3)2CHCH2OH或CH3CH2CH2CH2OH,對應的A為(CH3)3COH或CH3CH2CH(OH)CH3,對應C為(CH3)2CHCHO或CH3CH2CH2CHO,C發生氧化反應生成D,據此解答.
解答 解:Ⅰ、(1)A.由龍膽酸甲酯的結構可知,分子中含有酚羥基,具有酚的性質,能與氯化鐵溶液顯色,故A正確;
B.由龍膽酸甲酯的結構可知,分子中含有酯基、羥基,不含羧基,故B錯誤;
C.由龍膽酸甲酯的結構可知,分子中含有酚羥基,具有酚的性質,酚羥基的鄰位有H原子,能與溴水反應,故C正確;
D.由龍膽酸甲酯的結構可知,分子中含有酚羥基,酚羥基的酸性小于碳酸,與碳酸鈉反應生成碳酸氫鈉,故D錯誤;
故答案為:BD;
(2)龍膽酸甲酯與足量氫氧化鈉溶液發生水解反應,同時發生酚與氫氧化鈉的中和反應,反應的化學方程式為: ,
,
故答案為: ;
;
Ⅱ、X在稀硫酸、加熱條件下生成龍膽酸與A,為酯的水解反應,A為醇,A發生消去反應生成C4H8,A與B互為同分異構體,B能催化氧化生成C,C能發生銀鏡反應,故B中-OH連接的碳原子上含有2個H原子,B為(CH3)2CHCH2OH或CH3CH2CH2CH2OH,對應的A為(CH3)3COH或CH3CH2CH(OH)CH3,對應C為(CH3)2CHCHO或CH3CH2CH2CHO,C發生氧化反應生成D,
(3)X發生水解反應生成生成A與龍膽酸,屬于取代反應,A發生消去反應生成C4H8,C4H8發生加聚反應生成高分子化合物,C4H8發生加成反應生成C4H9Br,C4H9Br發生取代反應生成B,B發生氧化反應生成C,C反應氧化反應生成D,沒有涉及的反應類型是:還原反應,
故答案為:③;
(4)由上述分析可知,A為A為(CH3)3COH或CH3CH2CH(OH)CH3,X發生水解反應生成生成A與龍膽酸,故X的結構簡式是 ,
,
故答案為: .
.
點評 本題考查有機物的推斷、官能團的性質、同分異構體、有機反應類型等,難度中等,推斷B的結構是關鍵,注意掌握官能團的性質與轉化.


科目:高中化學 來源: 題型:解答題
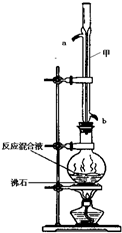 苯甲酸甲酯是一種重要的工業原料,某化學小組采用如圖裝置,以苯甲酸、甲醇為原料制取苯甲酸甲酯.有關物質的物理性質見下表所示:
苯甲酸甲酯是一種重要的工業原料,某化學小組采用如圖裝置,以苯甲酸、甲醇為原料制取苯甲酸甲酯.有關物質的物理性質見下表所示:| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔點/℃ | 122.4 | -97 | -12.3 |
| 沸點/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 弱酸化學式 | H2SO3 | H2CO3 |
| 電離常數(25℃) | Ka1=1.3×10-2 Ka2=6.3×10-8 | Ka1=4.2×10-7 Ka2=5.6×10-11 |
| A. | c(HCO3-)<c(CO32-) | |
| B. | 兩溶液都能使酸性高錳酸鉀溶液褪色 | |
| C. | c(HCO3-)>c(HSO3-) | |
| D. | c(CO32-)+c(HCO3-)=c(SO32-)+c(HSO3-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 醋酸的電離度 | B. | 溶液的導電性 | ||
| C. | 溶液的c(OH-) | D. | 溶液中$\frac{[C{H}_{3}COO].[{H}^{+}]}{[C{H}_{3}COOH]}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 氯元素是生產生活中常見的非金屬元素
氯元素是生產生活中常見的非金屬元素查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| Z | M | R | Q | |
| 原子半徑/nm | 0.186 | 0.074 | 0.099 | 0.143 |
| 主要化合價 | -2 | -1,+7 | +3 |
| A. | X與M形成的化合物中含有離子鍵 | |
| B. | Z、M、Q三種元素的簡單離子的半徑:M>Z>Q | |
| C. | Y與R形成的化合物中R呈正價,說明Y的非金屬性比R強 | |
| D. | 在元素周期表中,Q位于金屬與非金屬的交界處,可以作半導體材料 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4 L 的CCl4含有4NA個Cl原子 | |
| B. | 0.1 mol•L-1Na2S溶液中含有0.1NA個S2- | |
| C. | 常溫常壓下,92g的NO2和N2O4混合氣體含有的N原子數為2NA | |
| D. | 常溫常壓下,22.4L氯氣與足量的鐵粉反應,轉移的電子數為2NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com