
科目: 來源: 題型:選擇題
| A. | 中和時所需NaOH的量 | B. | 與Mg反應的起始速率 | ||
| C. | OH-的物質的量濃度 | D. | 溶液中$\frac{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$ |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 常溫下,pH=3和pH=5的鹽酸各10mL混合,所得溶液的pH=4 | |
| B. | 當溫度不變時,在純水中加入強堿溶液不會影響水的離子積常數 | |
| C. | 液氯雖然不導電,但溶解于水后導電情況良好,因此,液氯也是強電解質 | |
| D. | 溶液中c(H+)越大,pH也越大,溶液的酸性就越強 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 增大反應物濃度可以增大活化分子百分數,從而使反應速率增大 | |
| B. | 汽車尾氣的催化轉化裝置可將尾氣中的NO和CO等有害氣體快速地轉化為N2和CO2,其原因是催化劑可增大NO和CO反應的活化能 | |
| C. | 常溫下,反應C(s)+CO2(g)═2CO(g)不能自發進行,則該反應的△H>0 | |
| D. | 在“中和熱的測量實驗”中測定反應后溫度的操作方法:將量筒中的NaOH溶液經玻璃棒引流緩緩倒入盛有鹽酸的簡易量熱計中,立即蓋上蓋板,并用環形玻璃攪拌棒不斷攪拌,準確讀出并記錄反應體系的最高溫度 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 用A表示的反應速率是0.4 mol•(L•min)-1 | |
| B. | 2 min內,v正(B)和v逆(C)表示的反應速率的值都是逐漸減小的 | |
| C. | 2 min末的反應速率用B表示是0.3 mol•(L•min)-1 | |
| D. | 分別用B、C、D表示的反應速率其比值是3:2:1 |
查看答案和解析>>
科目: 來源: 題型:解答題
| 實驗編號 | T(K) | 催化劑 | CO2轉化率(%) | 甲醇選擇性(%) |
| 1 | 543 | 催化劑 A | 12.3 | 42.3 |
| 2 | 543 | 催化劑B | 10.9 | 72.7 |
| 3 | 553 | 催化劑 A | 15.3 | 39.1 |
| 4 | 553 | 催化劑B | 12.0 | 71.6 |
查看答案和解析>>
科目: 來源: 題型:解答題

| 編號 | 反應溫度/℃ | Na2S2O3濃液/mL | 甲 | 0.1mol/LH2SO4溶液/mL | 乙 |
| ① | 25℃ | 10.0 | 0 | 10.0 | |
| ② | 25℃ | 5.0 | a | 10.0 | |
| ③ | 45℃ | 10.0 | 0 | 10.0 |
查看答案和解析>>
科目: 來源: 題型:選擇題
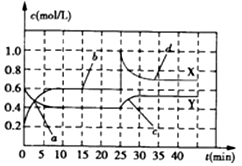
| A. | 前10min內用NO2表示的化學反應速率v(NO2)=0.02mol/(L•min) | |
| B. | 反應進行至25min時,曲線發生變化的原因可以是向容器中添加NO2(g) | |
| C. | 若要達到與最后相同的化學平衡狀態,在25min時還可以采取的措施是添加N2O4(g) | |
| D. | a、b、c、d四個點中,表示化學反應處于平衡狀態的點成是b和d |
查看答案和解析>>
科目: 來源: 題型:選擇題
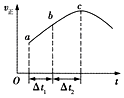 向絕熱恒容密閉容器中通入CO和H2O(g),在一定條件下使反應CO(g)+H2O(g)?CO2(g)+H2(g)達到判平衡,正反應速率隨時間變化的示意圖如圖所示.由圖可得出的正確結論是( )
向絕熱恒容密閉容器中通入CO和H2O(g),在一定條件下使反應CO(g)+H2O(g)?CO2(g)+H2(g)達到判平衡,正反應速率隨時間變化的示意圖如圖所示.由圖可得出的正確結論是( )| A. | 反應物的總能量低于生成物的總能量 | |
| B. | △t1=△t2時,CO的轉化率:a~b段小于b〜c段 | |
| C. | 反應在c點達到平衡狀態 | |
| D. | 反應物濃度:a點小于b點 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com