
科目: 來源: 題型:實驗題
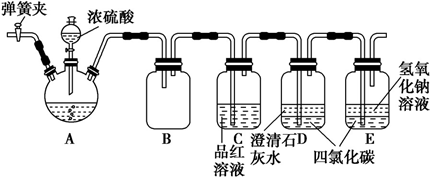
查看答案和解析>>
科目: 來源: 題型:解答題

 .
.查看答案和解析>>
科目: 來源: 題型:解答題
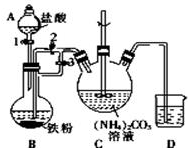 乳酸亞鐵{[CH3CH(OH)COO]2Fe}是一種很好的食品鐵強化劑,易溶于水,吸收效果比無機鐵好,可由乳酸與FeCO3反應制得.
乳酸亞鐵{[CH3CH(OH)COO]2Fe}是一種很好的食品鐵強化劑,易溶于水,吸收效果比無機鐵好,可由乳酸與FeCO3反應制得.查看答案和解析>>
科目: 來源: 題型:解答題
| v正 | v逆 | 平衡常數K | 轉化率α |
| 增大 | 增大 | 減小 | 減小 |
| [CO2]/mol•L-1 | [H2]/mol•L-1 | [CH4]/mol•L-1 | [H2O]/mol•L-1 | |
| 平衡Ⅰ | a | b | c | d |
| 平衡Ⅱ | m | n | x | y |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | a1、a2均減小 | B. | a1減小,a2增大 | C. | a1、不變,a2增大 | D. | a1不變,a2減小 |
查看答案和解析>>
科目: 來源: 題型:計算題
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 加入少量W,逆反應速率增大 | |
| B. | 因正反應吸熱,所以升高溫度正反應速率加快,逆反應速率減慢 | |
| C. | 當v(X)=v(Z)時,反應達到平衡 | |
| D. | 混合氣體的密度不變時,反應達到平衡 |
查看答案和解析>>
科目: 來源: 題型:實驗題
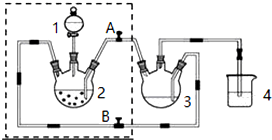
查看答案和解析>>
科目: 來源: 題型:實驗題
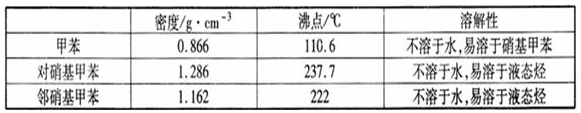
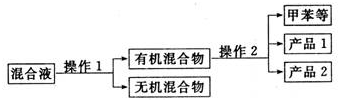
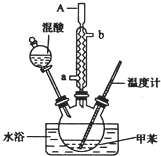 一硝基甲苯是一種重要的工業原料,某化學學習小組設計如圖所示裝置制備一硝基甲苯(包括對硝基甲苯和鄰硝基甲苯).反應原理:
一硝基甲苯是一種重要的工業原料,某化學學習小組設計如圖所示裝置制備一硝基甲苯(包括對硝基甲苯和鄰硝基甲苯).反應原理:
 .
.
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 平衡向正反應方向移動了 | B. | 物質R的轉化率減少了 | ||
| C. | 物質X的質量分數減少了 | D. | a+b<c+d |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com