
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
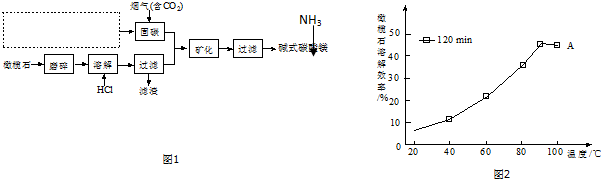
 .
.查看答案和解析>>
科目: 來源: 題型:解答題
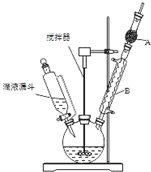 三苯甲醇(C6H5)3C-OH是一種重要的化工原料和醫藥中間體.實驗室合成三苯甲醇的實驗裝置如圖所示.
三苯甲醇(C6H5)3C-OH是一種重要的化工原料和醫藥中間體.實驗室合成三苯甲醇的實驗裝置如圖所示.| 物質 | 沸點/℃ |
| 三苯甲醇 | 380 |
| 乙醚 | 34.6 |
| 溴苯 | 156.2 |
查看答案和解析>>
科目: 來源: 題型:解答題
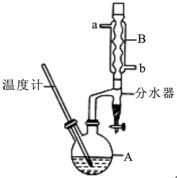 正丁醚常用作有機反應的溶劑.實驗室制備正丁醚的反應和主要實驗裝置如下:2CH3CH2CH2CH2OH$→_{△}^{濃硫酸}$CH3CH2CH2CH2)2O,反應物和產物的相關數據如下表:
正丁醚常用作有機反應的溶劑.實驗室制備正丁醚的反應和主要實驗裝置如下:2CH3CH2CH2CH2OH$→_{△}^{濃硫酸}$CH3CH2CH2CH2)2O,反應物和產物的相關數據如下表:| 相對分子質量 | 沸點/℃ | 密度/(g/cm3) | 水中的溶解性 | |
| 正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
| 正丁醚 | 130 | 142.0 | 0.7704 | 幾乎不溶 |
查看答案和解析>>
科目: 來源: 題型:解答題
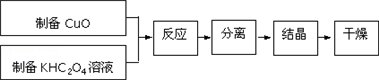
查看答案和解析>>
科目: 來源: 題型:解答題
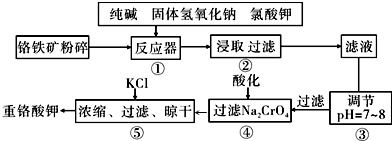
查看答案和解析>>
科目: 來源: 題型:解答題
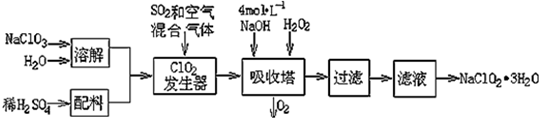
| 弱酸 | HClO2 | HF | HCN | H2S |
| Ka | 1×10-2 | 6.3×10-4 | 4.9×10-10 | K1=9.1×10-8 K2=1.1×10-12 |
查看答案和解析>>
科目: 來源: 題型:解答題
| 相對分子質量 | 熔點/℃ | 沸點/℃ | 溶解性 | |
| 甲苯 | 92 | -94.9 | 110.6 | 難溶于水 |
| 苯甲酸 | 122 | 122.13 | 249 | 微溶于水 |
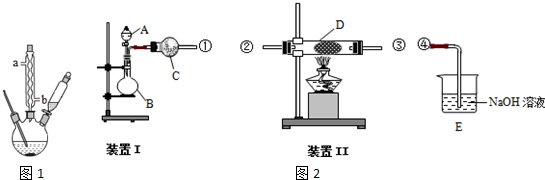
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
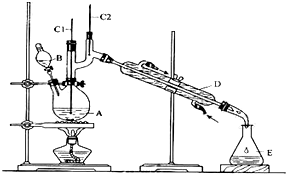
| 沸點/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 11.72 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com