
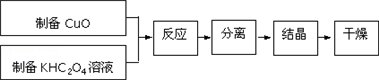
分析 (1)①過濾一般在漏斗中進行,且用玻璃棒引流,用燒杯盛裝濾液;
②CuO表面會附著硫酸根離子,用氯化鋇溶液檢驗最后一次洗滌液中是否含有硫酸根離子判斷是否洗滌干凈;
(2)①提高氧化銅的利用率,可用氧化銅與KHC2O4溶液充分反應;
②CuO與KHC2O4溶液在50℃水浴加熱條件下反應生成K2[Cu(C2O4)2]與H2O;
(3)從硫酸銅溶液中獲得硫酸銅晶體時,為減少硫酸銅的溶解,可用加入少量乙醇,并用蒸餾的方法分離乙醇.
解答 解:(1)①過濾裝置所需的玻璃儀器有漏斗、燒杯、玻璃棒,故答案為:漏斗、燒杯、玻璃棒;
②CuO表面會附著硫酸根離子,檢驗是否洗滌干凈的具體方法是:取最后一次洗滌濾液,滴入BaCl2溶液,若無白色沉淀,說明已洗滌干凈,
故答案為:取最后一次洗滌濾液,滴入BaCl2溶液,若無白色沉淀,說明已洗滌干凈;
(2)①過濾時濾紙上沾有大量的氧化銅固體,所以應直接將洗滌干凈的氧化銅固體連同濾紙一起加入到草酸氫鉀溶液中,充分反應后取出濾紙或將濾紙灼燒成灰再將剩余的固體轉入熱的KHC2O4溶液,
故答案為:ad;
②根據題意可知,CuO與KHC2O4溶液在50℃水浴加熱條件下反應生成K2[Cu(C2O4)2]與H2O,反應的方程式為:2KHC2O4+CuO$\frac{\underline{\;50℃\;}}{\;}$K2[Cu(C2O4)2]+H2O,
故答案為:2KHC2O4+CuO$\frac{\underline{\;50℃\;}}{\;}$K2[Cu(C2O4)2]+H2O;
(3)①從硫酸銅溶液中獲得硫酸銅晶體時,為減少硫酸銅的溶解,降低硫酸銅的溶解度,有利于硫酸銅晶體析出,可用加入少量乙醇,
故答案為:降低硫酸銅的溶解度,有利于硫酸銅晶體析出;
②在蒸發濃縮的初始階段還采用了蒸餾的方法,可起到回收乙醇的作用,故答案為:回收乙醇.
點評 本題考查物質的制備,為高頻考點,側重于學生的分析能力和實驗能力的考查,注意把握物質的性質以及實驗的原理和操作,難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | CH3COOH | B. | CH3COOCH2CH3 | C. | CH2=CHCOOH | D. | 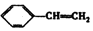 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 沸點/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 11.72 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 中子數為20的氯原子:${\;}_{17}^{37}$Cl | |
| B. | 次氯酸的電子式: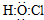 | |
| C. | 氮原子的結構示意圖: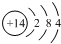 | |
| D. | 碳酸氫鈉的電離方程式:NaHCO3=Na++H++CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
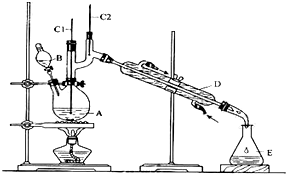
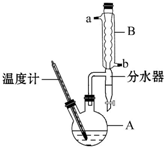 1-溴丙烷常用作有機反應的溶劑.實驗室制備1-溴丙烷(CH3CH2CH2Br)的反應和主要實驗裝置如圖:
1-溴丙烷常用作有機反應的溶劑.實驗室制備1-溴丙烷(CH3CH2CH2Br)的反應和主要實驗裝置如圖:| 相對分 子質量 | 密度 /g•mL-1 | 沸點/℃ | 水中 溶解性 | |
| 正丙醇 | 60 | 0.896 | 97.1 | 溶 |
| 正丙醚 | 102 | 0.74 | 90 | 幾乎不溶 |
| 1-溴丙烷 | 123 | 1.36 | 71 | 不溶 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
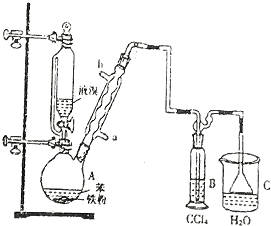
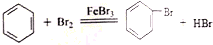 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應前后氣體的壓強之比為2:1 | |
| B. | 反應前后氣體的密度之比為15:16 | |
| C. | 此時CO的轉化率為50% | |
| D. | 如果反應繼續向正向進行,氣體的平均相對分子質量將減小 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com