
科目: 來源: 題型:多選題
| 溫度℃ | 400 | 500 | 830 | 1000 |
| 平均常數K | 10 | 9 | 1 | 0.6 |
| A. | 上述反應中正反應是吸熱反應 | |
| B. | 該反應的化學平衡常數表達式為K=$\frac{\{c({H}_{2})•c(C{O}_{2})\}}{\{c(CO)•c({H}_{2}O)\}}$ | |
| C. | 該反應在400℃時達平衡狀態,若升高溫度,則正反應速率減小,逆反應速率增大 | |
| D. | 在830℃,2L的密閉容器中,沖入1molCO、5molH2O(g)、3molCO2和2molH2發生上述反應,在達到平衡前V(正)<V(逆) |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 制取無水MgCl2,將MgCl2溶液直接蒸干 | |
| B. | 除去CuCl2溶液中含有的少量FeCl2,向溶液中加入過量CuO,待充分反應后過濾 | |
| C. | 的檢驗:取少量試樣于試管中,滴加鹽酸酸化的BaCl2溶液,有白色沉淀生成,則試樣中含有 | |
| D. | 探究反應的限度:將1mL0.1mol•L-1的KI溶液與5mL0.1mol•L-1的FeCl2溶液混合,待充分反應后,滴加KSCN溶液,觀察實驗現象 |
查看答案和解析>>
科目: 來源: 題型:解答題

查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | CO2、CH4、N2等均是造成溫室效應的氣體 | |
| B. | “地溝油”經過加工處理后,可以用來制造燃油 | |
| C. | 鐵粉、生石灰、硅膠是食品包裝中常用的干燥劑 | |
| D. | 目前加碘食鹽主要添加的是KI |
查看答案和解析>>
科目: 來源: 題型:選擇題
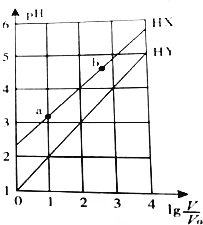
| A. | HX、HY都是弱酸,且HX的酸性比HY的弱 | |
| B. | 常溫下,由水電離出的c(H+)•c(OH-):a<b | |
| C. | 相同溫度下,電離常數K( HX):a>b | |
| D. | lg$\frac{V}{{V}_{0}}$=3,若同時微熱兩種溶液(不考慮HX、HY和H2O的揮發),則$\frac{c({X}^{-})}{c({Y}^{-})}$減小 |
查看答案和解析>>
科目: 來源: 題型:解答題
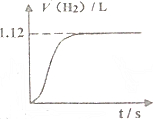 常溫下在1LpH=3的HA溶液中加入過量鐵粉,產生氫氣的體積隨時間變化的曲線如圖所示(氫氣體積已折算成標準狀況下的體積)
常溫下在1LpH=3的HA溶液中加入過量鐵粉,產生氫氣的體積隨時間變化的曲線如圖所示(氫氣體積已折算成標準狀況下的體積)查看答案和解析>>
科目: 來源: 題型:填空題
 實驗室需要0.1mol/L NaOH溶液450mL,需要0.5mol/L硫酸溶液500mL.根據這兩種溶液的配置情況回答下列問題:
實驗室需要0.1mol/L NaOH溶液450mL,需要0.5mol/L硫酸溶液500mL.根據這兩種溶液的配置情況回答下列問題:查看答案和解析>>
科目: 來源: 題型:解答題
| 物質 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| 溶解度 (g/100g水) | 0 | 28 | 35.7 | 4.7 | 163 |
| 40 | 40.1 | 36.4 | 26.3 | 215 | |
| 80 | 51.3 | 38 | 73 | 376 | |
查看答案和解析>>
科目: 來源: 題型:解答題

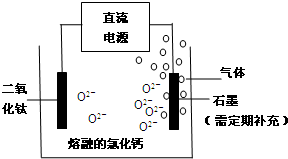
查看答案和解析>>
科目: 來源: 題型:填空題
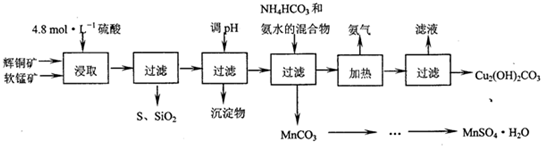
| 開始沉淀的PH | 沉淀完全的PH | |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com