
科目: 來源: 題型:解答題
 在化學研究領域,經常需要對一些物質進行性質的確定.如利用下列裝置(夾持儀器已略去)測出一定質量鎂與鹽酸反應放出的氣體體積,對金屬鎂的相對原子質量進行測定,實驗步驟如下:
在化學研究領域,經常需要對一些物質進行性質的確定.如利用下列裝置(夾持儀器已略去)測出一定質量鎂與鹽酸反應放出的氣體體積,對金屬鎂的相對原子質量進行測定,實驗步驟如下:查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 反應N2(g)+3H2(g)═2NH3(g),其他條件不變時充入N2,正反應速率增大,逆反應速率減小 | |
| B. | 常溫下,2NO(g)+O2(g)═2NO2(g)能夠自發進行,則該反應的△H<0 | |
| C. | 向0.1mol/L CH3COOH溶液中加入少量的冰醋酸,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(O{H}^{-})}$的值變小 | |
| D. | 電解法精煉銅時,以粗銅作陰極,純銅作陽極 |
查看答案和解析>>
科目: 來源: 題型:解答題
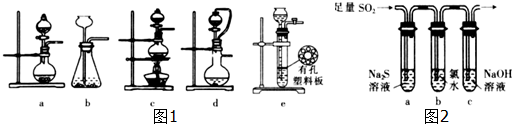
查看答案和解析>>
科目: 來源: 題型:解答題
| 第一電離能 | 鍵能 | 沸點 | 離子半徑 |
| Be>B | C-C>Si-Si | H2S<H2O | Al3+<O2- |
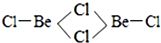
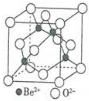
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 0.5 mol•L-1 NaOH溶液中Na+數為0.5NA | |
| B. | 標準狀況下,22.4 L四氯化碳含有的分子數為NA | |
| C. | 常溫常壓下,1mol Na2O2與足量CO2反應,電子轉移數為NA | |
| D. | 標準狀況下,16 g氧氣臭氧的混合氣體所含原子數一定為2NA |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 鈉鉀合金可用于中子反應堆作熱交換劑 | |
| B. | 氯氣本身有毒,因此不能用于藥物合成 | |
| C. | 不用氧化鎂電解熔融制鎂的原因是氧化鎂不導電 | |
| D. | 工業高爐煉鐵過程中,加石灰石主要是為了制備還原劑 |
查看答案和解析>>
科目: 來源: 題型:解答題
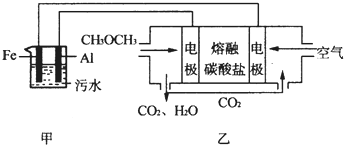
查看答案和解析>>
科目: 來源: 題型:解答題

查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com