
科目: 來源:2016屆湖北省黃岡市高三4月考試理綜化學試卷(解析版) 題型:選擇題
迷迭香酸有很強的抗氧化性,對癌癥和動脈硬化的預防起到一定作用,其結構如下圖所示。下列敘述正確的是( )
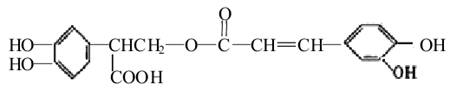
A.迷迭香酸的分子式為C18H15O8
B.迷迭香酸分子中含有5種官能團
C.1mol迷迭香酸跟H2反應,最多可消耗7mol H2
D.迷迭香酸能使酸性高錳酸鉀及溴的四氯化碳溶液褪色,屬于芳香烴
查看答案和解析>>
科目: 來源:2016屆湖北省黃岡市高三4月考試理綜化學試卷(解析版) 題型:選擇題
下列坐標圖均涉及到平衡原理,其中相關表述正確的是( )

A.圖②表示2SO2(g)+O2(g) 2SO3(g) △H<0正逆反應的平衡常數K隨溫度的變化
2SO3(g) △H<0正逆反應的平衡常數K隨溫度的變化
B.圖③表示反應2NH3(g) 3H2(g)+N2(g)在恒溫恒壓裝置中達平衡時,N2的物質的量與通入NH3的物質的量的變化關系
3H2(g)+N2(g)在恒溫恒壓裝置中達平衡時,N2的物質的量與通入NH3的物質的量的變化關系
C.圖④表示AgCl(s) Ag+(aq)+Cl-(aq)的離子的濃度關系,當處于b點時,蒸發部分的水后,可以到達平衡線的a點處
Ag+(aq)+Cl-(aq)的離子的濃度關系,當處于b點時,蒸發部分的水后,可以到達平衡線的a點處
D.圖①表示室溫下,用0.1mol·L-1氨水吸收HCl氣體時,溶液的粒子濃度隨吸收HCl的變化,實線表示c(NH3·H2O),虛線表示c(NH4+),處于M點時溶液呈中性
查看答案和解析>>
科目: 來源:2016屆湖北省黃岡市高三4月考試理綜化學試卷(解析版) 題型:選擇題
某溶液中含有NH4+、Fe2+、Al3+、SO42-、Cl-五種離子,若向其中加入過量的Na2O2,微熱并攪拌,再通入過量的HI氣體,充分反應后,最后加入足量的硝酸酸化的硝酸鋇溶液,則下列敘述不正確的是( )
A.反應后,溶液中NH4+、Fe2+、SO42-的物質的量減少,而Al3+、Cl-的物質的量不變
B.Fe2+先被氧化并形成沉淀,后來沉淀溶解并被還原為Fe2+,最后又被氧化
C.該實驗中共有二種氣體生成
D.Al3+先形成沉淀后溶解,后來再形成沉淀接著又沉淀溶解
查看答案和解析>>
科目: 來源:2016屆湖北省黃岡市高三4月考試理綜化學試卷(解析版) 題型:實驗題
苯胺為無色液體,還原性強,易被氧化;有堿性,與酸反應生成鹽。常用硝基苯與H2制備: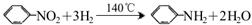 。
。
其部分裝置及有關數據如下:
沸點/℃ | 密度g/mL | 溶解性 | |
硝基苯 | 210.9 | 1.20 | 不溶于水,易溶于乙醇、乙醚 |
苯胺 | 184.4 | 1.02 | 微溶于水,易溶于乙醇、乙醚 |
乙醚 | 34.6 | 0.71 | 不溶于水,易溶于硝基苯、苯胺 |
實驗步驟:
①檢查裝置的氣密性,連接好C處冷凝裝置的冷水。
②先向三頸燒瓶中加入沸石及硝基苯,再取下恒壓分液漏斗,換上溫度計。
③打開裝置A、B間活塞,通入H2一段時間。
④點燃B處的酒精燈,加熱,使溫度維持在140℃進行反應。
⑤反應結束后,關閉裝置A、B間活塞,加入生石灰。
⑥調整好溫度計的位置,繼續加熱,收集182~186℃餾分,得到較純苯胺。
回答下列問題:
(1)步驟⑥中溫度計水銀球的位置在__________。
(2)下列關于實驗的敘述中,錯誤的是__________。
A.冷凝管的冷水應該從b進從a出
B.實驗開始酎,溫度計水銀球應插入反應液中,便于控制反應液的溫度
C.裝置A中應使用鋅粉,有利于加快生成H2的速率
D.加入沸石的目的是防止暴沸
(3)若實驗中步驟③和④的順序顛倒,則實驗中可能產生的后果是_____________。
(4)蒸餾前,步驟⑤中加入生石灰的作用是____________________。
(5)有學生質疑反應完成后,直接蒸餾得到苯胺的純度不高,提出以下流程:

苯胺在酸性條件下生成鹽酸苯胺被水萃取,在堿性溶液中又被放有機溶劑反萃取,這種萃取——反萃取法簡稱反萃。實驗中反萃的作用是__________;在分液漏斗中進行萃取分液時,應注意不時放氣,其目的是____________________。
(6)苯胺還原性強,易被氧化,請配平下列化學方程式的化學計量數。

查看答案和解析>>
科目: 來源:2016屆湖北省黃岡市高三4月考試理綜化學試卷(解析版) 題型:簡答題
利用含銅、鐵的粗鋅制備硫酸鋅及相關物質。工藝流程圖及有關數據如下:

物質 | Cu(OH)2 | Zn(OH)2 | Fe(OH)3 | ZnS | CuS |
Ksp | 5.0×10-20 | 2.0×10-16 | 4.0×10-38 | 1.2×10-23 | 8.5×10-45 |
請回答下列問題:
(1)粗鋅中的銅與混酸的稀溶液反應的化學方程式為__________________________,圖中處理氣體X要能夠體現綠色化學思想,還需補充氣體______(填化學式)。
(2)若溶液I中c(Cu2+)為0.05mol·L-1,則溶液II中c(Fe3+)>____mol·L-1。
(3)若固體A是Zn,取9.61 g固體C溶解于足量的500mL 2 mol·L-1稀硝酸中,共收集到標準狀況下2.24L的氣體,向所得溶液中加入2 mol·L-1 NaOH溶液,則當生成沉淀最多時,沉淀的質量為_____g;若固體A是另一種物質,取部分固體C于試管中,加入鹽酸產生有臭雞蛋味氣體,則該反應的離子方程式為________________________。
(4)溶液Ⅲ經過蒸發濃縮、____________、過濾、洗滌、干燥,即得到較純凈的硫酸鋅晶體;溶液還可以制備ZnS,實際選擇的是(NH4)2S溶液而不是Na2S溶液作為反應物,理由是后者制得的ZnS含有較多的雜質,則該雜質是____________(填化學式)。
(5)金屬鋅常用作酸性干電池的負極,干電池不使用時,由于負極與電解質溶液接觸而發生自放電反應:2NH4++Zn=2NH3+H2↑+Zn2+,造成電量自動減少。寫出鉛蓄電池不使用時,其正極上發生自放電的化學方程式__________________________。
查看答案和解析>>
科目: 來源:2016屆湖北省黃岡市高三4月考試理綜化學試卷(解析版) 題型:填空題
近幾年我國大面積發生霧霾天氣,其主要原因是SO2、NOx,揮發性有機物等發生二次轉化,研究碳、氮、硫及其化合物的轉化對于環境的改善有重大意義。
(1)在一定條件下,CH4可與NOx反應除去NOx,已知有下列熱化學方程式:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3 kJ·mol-1
②N2(g)+2O2(g) 2NO2(g) △H=+67.0 kJ·mol-1
2NO2(g) △H=+67.0 kJ·mol-1
③H2O(g)=H2O(l) △H=-41.0 kJ·mol-1
則CH4(g)+2NO2(g)  CO2(g)+2H2O(g)+N2 (g) △H=_____kJ·mol-1;
CO2(g)+2H2O(g)+N2 (g) △H=_____kJ·mol-1;
(2)在3.0 L密閉容器中,通入0.10 mol CH4和0.20 mol NO2,在一定溫度進行反應,反應時間(t)與容器內氣體總壓強(p)的數據見下表
時間t/min | 0 | 2 | 4 | 6 | 8 | 10 |
總壓強p/100kPa | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
由表中數據計算0~4min內v(NO2)=_________,該溫度下的平衡常數K=________。
(3)在一恒容裝置中,通入一定量CH4和NO2,測得在相同時間內,在不同溫度下,NO2的轉化率如圖(橫坐標為反應溫度,縱坐標為NO2轉化率/%):
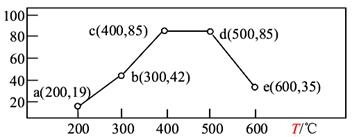
則下列敘述正確的是____________。
A.若溫度維持在200℃更長時間,NO2的轉化率將大于19%
B.反應速率:b點的v(逆)>e點的v(逆)
C.平衡常數:c點=d點
D.提高c點時NO2的轉化率和反應速率,可適當升溫或增大c(CH4)
(4)用0.05 mol·L-1Na2S溶液吸收上述甲烷中含有的H2S氣體,當吸收的H2S的物質的量與原Na2S的物質的量相等時溶液顯堿性,此時溶液中有關粒子的表達式正確的是( )
A.n(Na+)=0.1 mol B.c(Na+)-c(OH-)>c(S2-)+c(HS-)-c(H+)
C.c(H2S)+c(H+)<c(S2-)+c(OH-) D.c(Na+)-c(H2S)=2c(S2-)+c(HS-)
測得25℃時溶液中的c(H2S)=1.0×10-4mol·L-1,則溶液的pH=________。
(5)將(1)中CH4+2NO2 CO2+2H2O+N2的反應設計為原電池,電池內部是摻雜氧化釔的氧化鋯晶體,可以傳導O2-;則電池的正極電極反應式為______________。
CO2+2H2O+N2的反應設計為原電池,電池內部是摻雜氧化釔的氧化鋯晶體,可以傳導O2-;則電池的正極電極反應式為______________。
查看答案和解析>>
科目: 來源:2016屆湖北省黃岡市高三4月考試理綜化學試卷(解析版) 題型:簡答題
[化學—選修2:化學與技術]粉煤灰是燃煤電廠排出的主要固體廢物。我國火電廠粉煤灰的主要氧化物組成為SiO2、Al2O3、CaO等。一種利用粉煤灰制取氧化鋁的工藝流程如下 :
:
(1)粉煤灰研磨的目的是_______________________。
(2)第1次過濾時濾渣的主要成分有__________、__________(填化學式,下同),第3次過濾時濾渣的成分是__________。
(3)在104℃用硫酸浸取時,鋁的浸取率與時間關系如圖1,適宜的浸取時間為__________h;鋁的浸取率與 的關系如圖2所示,從浸取率角度考慮,三種助溶劑NH4F、KF及NH4F與KF的混合物,在
的關系如圖2所示,從浸取率角度考慮,三種助溶劑NH4F、KF及NH4F與KF的混合物,在 相同時,浸取率最高的是__________(填助溶劑化學式);用含氟的化合物作這種助溶劑的缺點是__________(舉一例)。
相同時,浸取率最高的是__________(填助溶劑化學式);用含氟的化合物作這種助溶劑的缺點是__________(舉一例)。

(4)流程中循環使用的物質有__________。(填化學式)
(5)用鹽酸溶解硫酸鋁晶體,再通入HCl氣體,析出AlCl3·6H2O,請簡要說明該過程能夠發生的原因____________________。
(6)用粉煤灰制取含鋁化合物的主要意義是____________________。
查看答案和解析>>
科目: 來源:2016屆湖北省黃岡市高三4月考試理綜化學試卷(解析版) 題型:填空題
(化學—選修3:物質結構與性質)
氮化硼(BN)被稱為一種“宇宙時代的材料”,具有很大的硬度。
(1)基態硼原子有__________個未成對電子,氮離子的電子排布式為__________。
(2)部分硼的化合物有以下轉化: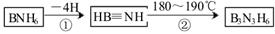
則下列敘述正確的是__________(填序號);
A.B3N3H6俗稱無機苯,但不是平面分子
B.BNH6與乙烷是等電子體
C.HB≡NH中的硼原子、氮原子韻雜化類型相同
D.硼、氮、氧三元素的第一電離能比較:B<N<O
(3)下圖的晶體結構中,黑球白球分別代表不同的原子、離子或分子,則圖1的晶胞中含有的粒子總數為__________;圖2中的白球的配位數是__________。
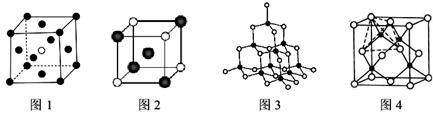
(4)已知圖3、4均表示BN晶體的結構,制備氮化硼的原理為:BCl3+2NH3=BN+2HCl+NH4Cl,當該反應中有1mol BN生成時,則反應中可形成__________mol配位鍵,比較氮化硼晶體與晶體硅的沸點高低并解釋原因____________________。
(5)X射線的衍射實驗可獲取晶體的結構,包括晶胞形狀、大小及原子的分布等參數,從而提供了又一種實驗測定阿伏加德羅常數和元素的相對質量的方法。若圖4晶胞的棱長為a nm,密度為ρ g·cm-3,則阿伏加德羅常數為__________(要求化為最簡關系)。
查看答案和解析>>
科目: 來源:2016屆湖北省黃岡市高三4月考試理綜化學試卷(解析版) 題型:推斷題
[化學—選修5:有機化學基礎]下圖為阿托酸甲酯的一種合成路線:

請回答下列問題:
(1)已知A為芳香烴,其核磁共振氫譜中出現5個蜂,其面積比為1∶1∶2∶2∶2,則A的名稱為__________,若要檢驗有機物B的官能團,則所使用的試劑除了有機物B和水之外,還需要的試劑有__________(填化學式)。
(2)寫出有關的化學方程式
反應②______________________________;
反應③______________________________。
(3)阿托酸甲酯所含官能團的名稱為__________;阿托酸甲酯有多種同分異構體,其中苯環上只有一個支鏈,既能與NaHCO3溶液反應,又能使溴的四氯化碳溶液褪色的同分異構體有__________種(不考慮立體異構)。
(4)阿托酸甲酯的另外一種合成路線如下圖所示:

已知在多步反應過程中進行了下列4種不同的反應類型,請按照實際進行的反應順序依次寫出這四種反應類型的字母序號__________。
A.取代反應 B.消去反應 C.加成反應 D.氧化反應
查看答案和解析>>
科目: 來源:2016屆遼寧省高三下第四次模擬理綜化學試卷(解析版) 題型:選擇題
化學與社會、生活、生產聯系廣泛。下列說法正確的是( )
A.高鐵酸鉀處理水的原理與明礬完全相同
B.推廣煤的氣化和液化技術,能減少二氧化碳的排放
C.“遼寧艦”上用于艦載機降落攔阻索的特種鋼纜屬于新型無機非金屬材料
D.食品安全包括限制添加劑的種類和添加的量
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com