
某溶液中含有NH4+、Fe2+、Al3+、SO42-、Cl-五種離子,若向其中加入過量的Na2O2,微熱并攪拌,再通入過量的HI氣體,充分反應后,最后加入足量的硝酸酸化的硝酸鋇溶液,則下列敘述不正確的是( )
A.反應后,溶液中NH4+、Fe2+、SO42-的物質的量減少,而Al3+、Cl-的物質的量不變
B.Fe2+先被氧化并形成沉淀,后來沉淀溶解并被還原為Fe2+,最后又被氧化
C.該實驗中共有二種氣體生成
D.Al3+先形成沉淀后溶解,后來再形成沉淀接著又沉淀溶解
 優等生題庫系列答案
優等生題庫系列答案 53天天練系列答案
53天天練系列答案科目:高中化學 來源:2016屆江西省高三5月模擬考試理綜化學試卷(解析版) 題型:實驗題
某學習小組研究溶液中Fe2+的穩定性;進行如下實驗,觀察,記錄結果。
實驗I
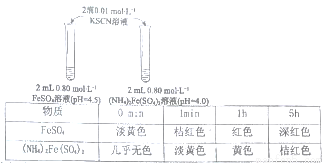
(1)上述(NH4)2Fe(SO4)2溶液pH小于FeSO4的原因是_____________(用化學用語表示)。溶液的穩定性:FeSO4_______(NH4)2Fe(SO4)2(填“>”或“<”)。
(2)甲同學提出實驗I中兩溶液的穩定性差異可能是(NH4)2Fe(SO4)2溶液中的NH4+保護了Fe2+,因為NH4+有還原性,進行實驗Ⅱ,否定了該觀點,補全該實驗。

(3)乙同學提出實驗I中兩溶液的穩定性差異是溶液酸性不同導致,進行實驗Ⅲ;分別配制0.80mol•L-1pH為1、2、3、4的FeSO4溶液,發現pH=1的FeSO4溶液長時間無明顯變化,pH越大,FeSO4溶液變黃的時間越短。
資料顯示:亞鐵鹽溶液中存在反應 4Fe2++O2+10H2O 4Fe(OH)3+8H+ 由實驗Ⅲ,乙同學可得出的結論是_________,原因是_________。
4Fe(OH)3+8H+ 由實驗Ⅲ,乙同學可得出的結論是_________,原因是_________。
(4)進一步研究在水溶液中Fe2+的氧化機理,測定同濃度FeSO4溶液在不同pH條件下,Fe2+的氧化速率與時間的關系如圖(實驗過程中溶液溫度幾乎無變化)。反應初期,氧化速率逐漸增大的原因可能是_________。
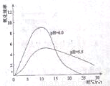
(5)綜合以上實驗,增強Fe2+穩定性的措施有_________。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年重慶市高二下期中化學試卷(解析版) 題型:選擇題
甲醛(H2C=O)在Ni催化作用下加氫可得到甲醇(CH3OH),以下說法中正確的是
A.甲醇、甲醛分子間都可以形成氫鍵
B.甲醇分子內C原子采取sp2雜化,O原子采取sp雜化
C.甲醛為極性分子,分子中兩個C—H鍵夾角小于120°
D.甲醇分子內的O—C—H鍵角大于甲醛分子內的O—C—H鍵角
查看答案和解析>>
科目:高中化學 來源:2016屆遼寧省高三下第四次模擬理綜化學試卷(解析版) 題型:選擇題
青銅器的制造是中華民族勞動人民智慧的結晶,成為一個時代的象征,但出土的青銅器大多受到環境腐蝕。如圖為青銅器在潮濕環境中發生電化學腐蝕的原理示意圖。環境中的 Cl- 擴散到孔口,并與各電極產物作用生成多孔粉狀銹 Cu2(OH)3Cl 。
下列說法不正確的是( )
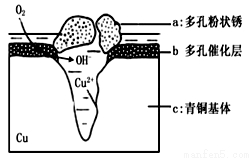
A. 腐蝕過程中,負極 a被氧化
B. 環境中的Cl-擴散到孔口,并與正極反應產物和負極
反應產物作用生成多孔粉狀銹Cu2(OH)3Cl,其離子方程式為2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓
C. 若生成 2.145gCu2(OH)3Cl,則理論上消耗標準狀況氧氣體積為 0.448L
D. 正極的電極反應式為: 正極反應是 O2+ 4e-+2H2O=4OH-
查看答案和解析>>
科目:高中化學 來源:2016屆湖北省黃岡市高三4月考試理綜化學試卷(解析版) 題型:填空題
(化學—選修3:物質結構與性質)
氮化硼(BN)被稱為一種“宇宙時代的材料”,具有很大的硬度。
(1)基態硼原子有__________個未成對電子,氮離子的電子排布式為__________。
(2)部分硼的化合物有以下轉化: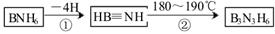
則下列敘述正確的是__________(填序號);
A.B3N3H6俗稱無機苯,但不是平面分子
B.BNH6與乙烷是等電子體
C.HB≡NH中的硼原子、氮原子韻雜化類型相同
D.硼、氮、氧三元素的第一電離能比較:B<N<O
(3)下圖的晶體結構中,黑球白球分別代表不同的原子、離子或分子,則圖1的晶胞中含有的粒子總數為__________;圖2中的白球的配位數是__________。
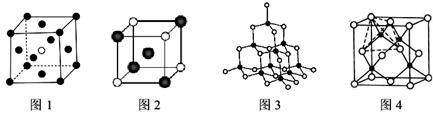
(4)已知圖3、4均表示BN晶體的結構,制備氮化硼的原理為:BCl3+2NH3=BN+2HCl+NH4Cl,當該反應中有1mol BN生成時,則反應中可形成__________mol配位鍵,比較氮化硼晶體與晶體硅的沸點高低并解釋原因____________________。
(5)X射線的衍射實驗可獲取晶體的結構,包括晶胞形狀、大小及原子的分布等參數,從而提供了又一種實驗測定阿伏加德羅常數和元素的相對質量的方法。若圖4晶胞的棱長為a nm,密度為ρ g·cm-3,則阿伏加德羅常數為__________(要求化為最簡關系)。
查看答案和解析>>
科目:高中化學 來源:2016屆湖北省黃岡市高三4月考試理綜化學試卷(解析版) 題型:選擇題
用相對分子質量為43的烷基取代烷烴(C4H10)分子中的一個氫原子,所得的有機物有(不考慮立體異構)( )
A.5種 B.7種 C.8種 D.4種
查看答案和解析>>
科目:高中化學 來源:2016屆河北省高三模擬押題理綜化學試卷(解析版) 題型:實驗題
NCl3可用于漂白,也可用于檸檬等水果的熏蒸處理。已知:NCl3熔點為-40℃,沸點為70℃,95℃以上易爆炸,有刺激性氣味,可與水反應。實驗室中可用氯氣和氨氣反應制取NCl3,反應方程式為4NH3+3C12===NCl3+3NH4Cl。某校化學興趣小組同學設計了如圖所示的實驗裝置(NH4Cl的分解溫度為300℃左右)。
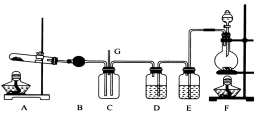
回答下列問題:
(1)寫出裝置F中的燒瓶內發生反應的離子方程式:___________________________。
(2)E中的試劑為__________________。
(3)導管G末端應連接的裝置為下圖中的___________(填選項字母)。
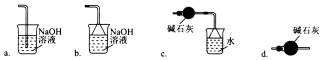
(4)NCl3遇水可發生水解反應生成兩種物質,其中一種是可使濕潤的紅色石蕊試紙變藍的氣體,寫出NCl3水解的化學方程式:_______________。
(5)已知C中生成的NH4Cl溶解在NCl3中,欲將二者分離可采取的操作方法為_____________________。
(6)NH4Al(SO4)2也可用于自來水的凈化。
①NH4Al(SO4)2溶液中離子濃度由大到小的順序為_________________。
②向NH4Al(SO4)2溶液中滴加氨水至溶液呈中性,在此過程中水的電離程度_________(填“增大”“減小”或“不變”)。
③常溫下,將a mol NH4Al(SO4)2:加入到b L c mol/L的氨水中,所得溶液呈中性,此時溶液中c(Al3+)≈0 mol/L,計算該溫度下NH3·H2O的電離常數___________(用含字母的代數式表示,忽略溶液體積變化)。
查看答案和解析>>
科目:高中化學 來源:2016屆福建師大附中高三下學期模擬考試理綜化學試卷(解析版) 題型:選擇題
短周期元素X、Y、Z、G、M的原子序數依次增大,X、Z同主族,可形成離子化合物ZX,Y單質是空氣的主要成分之一,可形成MY2、MY3兩種分子,G為金屬元素。下列判斷錯誤的是
A.原子半徑:Z>G>M>Y
B.G與Y形成的化合物一定既能與鹽酸反應,又能與燒堿溶液反應
C.X、Z分別與Y可形成原子數為1:1的物質
D.X、M形成的簡單陰離子的還原性:X > M
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高二下期中化學試卷(解析版) 題型:選擇題
一定溫度下,下列溶液的離子濃度關系式正確的是( )
A.pH=5的H2S溶液中,c(H+)=c(HS﹣)=1×10﹣5mol•L﹣1
B.pH=a的氨水溶液,稀釋10倍后,其pH=b,則a=b+1
C.pH=2的H2C2O4溶液與pH=12的NaOH溶液任意比例混合:
c(Na+)+c(H+)=c(OH﹣)+c(HC2O4-)
D.pH相同的①CH3COONa②NaHCO3③NaClO三種溶液的c(Na+):①>②>③
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com