
科目: 來源: 題型:
 如圖為實驗室某濃鹽酸試劑瓶標簽上的有關數據,試根據標簽上的有關數據,回答下列問題:
如圖為實驗室某濃鹽酸試劑瓶標簽上的有關數據,試根據標簽上的有關數據,回答下列問題:查看答案和解析>>
科目: 來源: 題型:
查看答案和解析>>
科目: 來源: 題型:
 某興趣小組設計研究銅和稀硝酸反應速率[v (NO)]的實驗.試回答下列問題:
某興趣小組設計研究銅和稀硝酸反應速率[v (NO)]的實驗.試回答下列問題:查看答案和解析>>
科目: 來源: 題型:
| 反應進程(分鐘) | 1 | 2 | 5 | 15 | 20 |
| 3.0mol/L鹽酸 | 少量氣泡 | 較多氣泡 | 大量氣泡 | 反應劇烈 | 鋁片耗盡 |
| 1.5mol/L硫酸 | 均無明顯現象(無氣泡產生) | ||||
| 3.0mol/L硫酸 | 均無明顯現象(無氣泡產生) | ||||
查看答案和解析>>
科目: 來源: 題型:
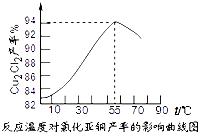 氯化亞銅(Cu2Cl2)是一種重要的化工產品,常用作有機合成催化劑.已知:
氯化亞銅(Cu2Cl2)是一種重要的化工產品,常用作有機合成催化劑.已知: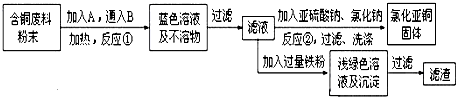
查看答案和解析>>
科目: 來源: 題型:
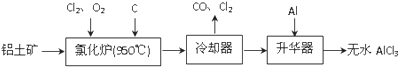
查看答案和解析>>
科目: 來源: 題型:
| 實驗 序號 | 金屬質量/g | 金屬 狀態 | C(H2SO4) /mol?L-1 | V(H2SO4) /mL | 溶液溫度/℃ | 金屬消 失的時 間/s | |
| 反應前 | 反應后 | ||||||
| 1 | 0.10 | 絲 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 絲 | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.10 | 絲 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.10 | 絲 | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.10 | 絲 | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | 絲 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 絲 | 1.1 | 50 | 30 | 44 | 40 |
查看答案和解析>>
科目: 來源: 題型:
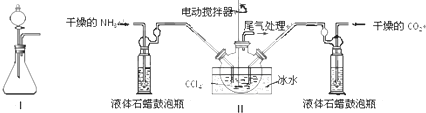
| 實驗步驟 | 預期現象和結論 |
| 步驟1:取少量固體樣品于試管中,加入蒸餾水至固體溶解. | 得到無色溶液 |
| 步驟2:向試管中加入過量的BaCl2溶液,靜置 | 若溶液不變渾濁,證明固體中不含碳酸銨. |
| 步驟3:向試管中繼續加入 |
查看答案和解析>>
科目: 來源: 題型:
| 二氧化錳與氯酸鉀的質量比 | 1/40 | 1/20 | 1/10 | 1/5 | 1/3 | 1/2 | 2/3 | 1/1 | 2/1 |
| 生成1L氧氣所需的時間(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
查看答案和解析>>
科目: 來源: 題型:
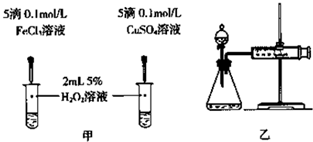
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com