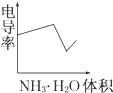
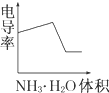
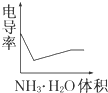
分析:(I)(1)膽礬固體放入燒杯中,加水制成溶液時需要用玻璃棒攪拌,加速膽礬固體溶解速度;在蒸發時用玻璃棒攪拌,是為了防止局部溫度過高使液滴飛濺;過濾時用到玻璃棒的作用是引流;氧化銅固體和一定質量的氯酸鉀固體,混合均勻也需要玻璃棒的攪拌;
(2)ag膽礬中含銅元素質量為ag×
=
a,設能制得氧化銅的質量為X,根據銅守恒由X×
═
a解得X=
a,所以由膽礬制備氧化銅的產率:
×100%=
;
(3)由于需要證明反應前后氧化銅的質量不變,反應后先將氧化銅從混合物中分離出來:加水溶解,進行過濾,得到的氧化銅上有氯化鉀溶液,進行洗滌干燥,再進行稱量即可;
(4)通過對比實驗才能說明氧化銅的確加快了氯酸鉀的反應速度,另取相同質量的氯酸鉀固體,不加氧化銅直接加熱,對比放出氧氣的速率快慢,現象很明顯.
(II)(1)根據n=c×V計算溶質的物質的量,配制硫酸銅溶液可以用硫酸銅,也可以用膽礬,根據m=n×M計算各自質量,配制溶液時注意水的體積不等于溶液的體積;
(2)根據實驗步驟進行分析;
(3)根據實驗步驟選擇儀器;
(4)根據C=
判斷濃度的變化.
解答:
解:(I)(1)膽礬固體放入燒杯中,加水制成溶液時需要用玻璃棒攪拌,加速膽礬固體溶解速度;在蒸發時用玻璃棒攪拌,是為了防止局部溫度過高使液滴飛濺;過濾時用到玻璃棒的作用是引流;氧化銅固體和一定質量的氯酸鉀固體,混合均勻也需要玻璃棒的攪拌,所以選擇①②③④,故答案為:①②③④;
(2)ag膽礬中含銅元素質量為ag×
=
a,設能制得氧化銅的質量為X,根據銅守恒由X×
═
a解得X=
a,所以由膽礬制備氧化銅的產率:
×100%=
,故答案為:
;
(3)由于需要證明反應前后氧化銅的質量不變,反應后先將氧化銅從混合物中分離出來:加水溶解,進行過濾,得到的氧化銅上有氯化鉀溶液,進行洗滌干燥,再進行稱量,故答案為:cadbe;
(4)通過對比實驗才能說明氧化銅的確加快了氯酸鉀的反應速度,另取相同質量的氯酸鉀固體,不加氧化銅直接加熱,對比放出氧氣的速率快慢,現象很明顯,
故答案為:對比實驗,稱取相等質量的氯酸鉀,加熱,比較產生相同體積氧氣所需的時間,或比較在相同時間內產生氧氣的體積.
(II)(1)配制200mL 1mol?L
-1的CuSO
4溶液,應選用250ml的容量瓶配置250ml,則溶質的物質的量為:n=c×V=0.25L×1mol/L=0.25mol,需要溶質的質量為:m(CuSO
4)=0.25mol×160g/mol=40g,或m(CuSO
4?5H
20)=0.25mol×250g/mol=62.5g.
A、應稱取40g無水硫酸銅,配成250mL溶液,故A錯誤;
B、250mL的容量瓶中配不到200mL溶液,故B錯誤;
C、應稱取40g無水硫酸銅,配成250mL溶液,水的體積不等于溶液的體積,故C錯誤;
D、稱取62.5gCuSO
4?5H
2O,在250mL的容量瓶中配成250mL溶液,故D正確.
故選D;
(2)物質的量濃度思維配置步驟一般為稱量、溶解、轉移、洗滌、定容、搖勻,故答案為:DAFCBE;
(3)根據實驗步驟選用的主要儀器有天平、鑰匙、玻璃棒、燒杯、250mL容量瓶、膠頭滴管,故答案為:玻璃棒、250mL容量瓶、膠頭滴管;
(4)①如果不冷卻,則熱的溶液轉移到容量瓶中,由于熱脹冷縮等到室溫時體積偏小,根據C=
,濃度偏高,故答案為:偏高;
②洗滌液轉入容量瓶后要振蕩,若不振蕩會使溶液體積偏小,根據C=
,濃度偏高,故答案為:偏高;
③若仰視會使體積偏大,根據C=
,濃度偏低,故答案為:偏低;
④用膠頭滴管向容量瓶中加水時,不慎超過刻度線,用膠頭滴管從瓶中吸出部分溶液使剩余溶液剛好達刻度線,會使溶質變少,根據C=
,濃度偏低,故答案為:偏低;
⑤使用潔凈的容量瓶前,瓶中殘留有少量蒸餾水,不會產生影響,故答案為:無影響.



 輕松課堂單元期中期末專題沖刺100分系列答案
輕松課堂單元期中期末專題沖刺100分系列答案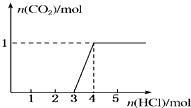 一定量CO2通入某濃度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀鹽酸,加入n(HCl)與生成n(CO2)的關系如圖所示.下列有關敘述正確的是( )
一定量CO2通入某濃度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀鹽酸,加入n(HCl)與生成n(CO2)的關系如圖所示.下列有關敘述正確的是( ) 常溫下,向25mL 0.1mol/LMOH溶液中逐滴加入0.2mol/L HA溶液,曲線如圖所示(假設混合后溶液體積的微小變化忽略不計).回答下列問題:
常溫下,向25mL 0.1mol/LMOH溶液中逐滴加入0.2mol/L HA溶液,曲線如圖所示(假設混合后溶液體積的微小變化忽略不計).回答下列問題: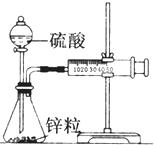 某化學興趣小組的甲、乙兩位同學對測定化學反應速率非常感興趣,為此進行了有關的實驗探究,實驗記錄如下.
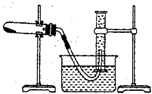
某化學興趣小組的甲、乙兩位同學對測定化學反應速率非常感興趣,為此進行了有關的實驗探究,實驗記錄如下.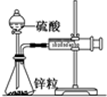 某溫度下按如圖安裝好實驗裝置,在錐形瓶內盛6.5g鋅粒(顆粒大小基本相同),通過分液漏斗加入40mL 2.5mol?L-1的硫酸,將產生的H2收集在一個注射器中,用時10s時恰好收集到氣體的體積為50mL(若折合成0℃、101kPa條件下的H2體積為44.8mL),在該溫度下,下列說法不正確的是( )
某溫度下按如圖安裝好實驗裝置,在錐形瓶內盛6.5g鋅粒(顆粒大小基本相同),通過分液漏斗加入40mL 2.5mol?L-1的硫酸,將產生的H2收集在一個注射器中,用時10s時恰好收集到氣體的體積為50mL(若折合成0℃、101kPa條件下的H2體積為44.8mL),在該溫度下,下列說法不正確的是( ) 電導率是衡量電解質溶液導電能力大小的物理量,根據溶液電導率變化可以確定滴定反應的終點.如圖是用KOH溶液分別滴定HCl溶液和CH3COOH溶液的滴定曲線示意圖.
電導率是衡量電解質溶液導電能力大小的物理量,根據溶液電導率變化可以確定滴定反應的終點.如圖是用KOH溶液分別滴定HCl溶液和CH3COOH溶液的滴定曲線示意圖.