
 電導率是衡量電解質溶液導電能力大小的物理量,根據溶液電導率變化可以確定滴定反應的終點.如圖是用KOH溶液分別滴定HCl溶液和CH3COOH溶液的滴定曲線示意圖.
電導率是衡量電解質溶液導電能力大小的物理量,根據溶液電導率變化可以確定滴定反應的終點.如圖是用KOH溶液分別滴定HCl溶液和CH3COOH溶液的滴定曲線示意圖.A、 |
B、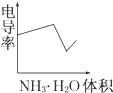 |
C、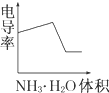 |
D、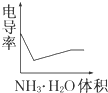 |


 名師點睛字詞句段篇系列答案
名師點睛字詞句段篇系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| ||
| 實驗步驟 | 預期現象與結論 |
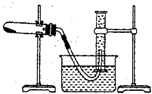
| 步驟I:取少量樣品于一支試管中,向其中加入適量 ,塞上帶導管的單孔塞,將導管另一端插入盛有足量 的試管中 | |
| 步驟II: |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
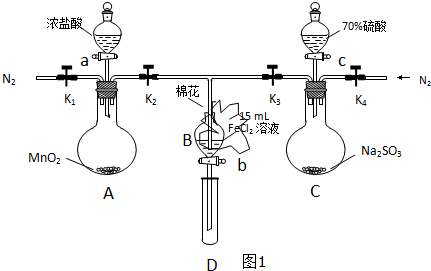
| 過程ⅣB溶液中含有的離子 | 過程ⅥB溶液中含有的離子 | |
| 甲 | 有Fe3+無Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+無Fe2+ | 有Fe2+ |
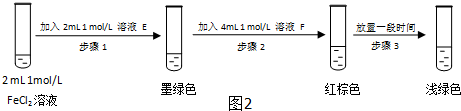
查看答案和解析>>
科目:高中化學 來源: 題型:
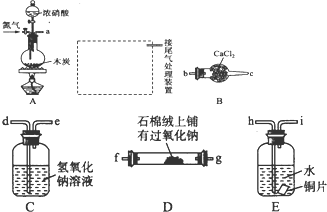
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、鹽溶液都是中性的 |
| B、鹽溶液的酸堿性與鹽的類型無關 |
| C、NaHCO3溶液顯酸性 |
| D、碳酸鈉溶液顯堿性,溶液中c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、等濃度的NH4HSO4、NH3?H2O、(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2的五種溶液,其中(NH4)2Fe(SO4)2溶液中c(NH4+)最大 |
| B、NaClO和BaCl2混合溶液:c(Na+)+2c(Ba2+)=c(ClO-)+c(HClO)+c(Cl-) |
| C、25℃下,0.2 mol?L-1 HCl溶液與0.2 mol?L-1 YOH(一元弱堿)溶液等體積混合(忽略混合后溶液體積的變化),則c(Cl-)=c(Y+)+c(YOH)=0.2 mol?L-1 |
| D、常溫下,將0.2 mol?L-1某一元堿ROH溶液和0.1 mol?L-1HCl溶液等體積混合,混合后溶液pH<7,則c(ROH)>c(R+) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com