
| A. | 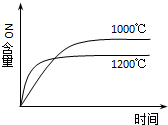 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-a kJ•mol-1 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-a kJ•mol-1 | |
| B. | 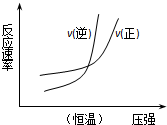 N2(g)+3H2(g)?2NH3(g)△H=-b kJ•mol-1 N2(g)+3H2(g)?2NH3(g)△H=-b kJ•mol-1 | |
| C. | 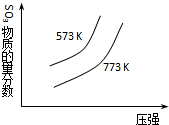 2SO3(g)?2SO2(g)+O2(g)△H=+c kJ•mol-1 2SO3(g)?2SO2(g)+O2(g)△H=+c kJ•mol-1 | |
| D. | 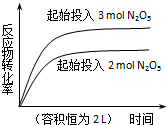 2N2O5(g)?4NO2(g)+O2(g)△H=+d kJ•mol-1 2N2O5(g)?4NO2(g)+O2(g)△H=+d kJ•mol-1 |
分析 A.該反應的正反應是放熱反應,升高溫度,平衡逆向移動,NO的含量減小;
B.該反應是一個反應前后氣體計量數之和減小的可逆反應,恒溫條件下,增大壓強,正逆反應速率都增大,平衡向正反應方向移動,則正反應速率大于逆反應速率;
C.該反應的正反應是吸熱反應,升高溫度,平衡正向移動,則三氧化硫含量降低;
D.該反應的正反應是反應前后氣體計量數之和增大的可逆反應,恒容條件下,增大反應物濃度,相當于增大壓強,平衡逆向移動.
解答 解:A.該反應的正反應是放熱反應,升高溫度,平衡逆向移動,NO的含量減小,但反應速率增大,反應達到平衡時間減小,符合圖象,故A正確;
B.該反應是一個反應前后氣體計量數之和減小的可逆反應,恒溫條件下,增大壓強,正逆反應速率都增大,平衡向正反應方向移動,則正反應速率大于逆反應速率,所以正逆反應速率相等后,正反應速率曲線在上面,故B錯誤;
C.該反應的正反應是吸熱反應,升高溫度,平衡正向移動,則三氧化硫含量降低,所以773K的曲線縱坐標小于573K的,符合圖象,故C正確;
D.該反應的正反應是反應前后氣體計量數之和增大的可逆反應,恒容條件下,增大反應物濃度,相當于增大壓強,平衡逆向移動,則五氧化二氮的轉化率降低,圖象不符合,故D錯誤;
故選AC.
點評 本題考查圖象分析,側重考查影響化學平衡移動因素、化學反應速率影響因素,明確外界條件對反應速率及平衡移動的影響原理是解本題關鍵,易錯選項是B,注意:反應速率圖象中,哪個方向反應速率較大,平衡就向哪個方向移動.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 達到化學平衡時,υ正(NH3)=υ逆(H2O) | |
| B. | 達到化學平衡時,4υ (O2)=5υ (NO) | |
| C. | 若單位時間內生成x mol NO的同時,也消耗x mol NH3 | |
| D. | 若單位時間內生成4 mol NO的同時,也生成4 mol NH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
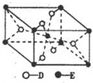
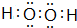 ,E的基態原子的外圍電子排布式為3d24s2.
,E的基態原子的外圍電子排布式為3d24s2.| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 室溫下pH=2的醋酸與pH=12的NaOH溶液等體積混合,所得溶液中:c(Na+)>c(OH)>c(CH3COO-)>c(H+) | |
| B. | 含KI、KCl均為0.1mol•L-1的混合溶液10mL與20mL0.1mol.L-1AgNO3溶液混合,所得懸濁液中:c(K+)═c(NO3-)>c(Ag+)>c(Cl-)>c(I-) | |
| C. | 室溫下,向10mL0.1mol•L-1的氨水中滴加同體積同濃度的CH3COOH的溶液,在滴加過程中:$\frac{c(N{{H}_{4}}^{+)}}{c(N{H}_{3}•{H}_{2}O)}$先增大再減小 | |
| D. | CH3COONa和CaCl2混合溶液中:c(Na+)+c(Ca2+)═c(CH3COO-)+(CH3COOH)+2c(Cl-) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com