
| 實驗 | 操作 | |
| A | 制取氫氧化鐵膠體 | 向沸騰的蒸餾水中按適當比例滴加FeCl3飽和溶液,繼續加熱至液體呈紅褐色,停止加熱 |
| B | 稀釋濃硫酸 | 先將濃硫酸加入燒杯中,后倒入蒸餾水 |
| C | 濃氨水與生石灰反應制備干燥的NH3 | 氣體產物通過濃硫酸后,用向下排空氣法收集 |
| D | 分離乙酸乙酯和飽和碳酸鈉溶液 | 從分液漏斗上口倒出有機層,再從下口放出水層 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.制備氫氧化鐵膠體時,需要將FeCl3飽和溶液加入沸水中并加熱;
B.濃硫酸的密度大于水,且稀釋過程中放出大量熱,應該將濃硫酸加入水中;
C.氨氣呈堿性,能夠與硫酸反應,不能用濃硫酸干燥;
D.飽和碳酸鈉溶液在下層,應該先從分液漏斗下口放出水層,然后再倒出有機層.
解答 解:A.制取氫氧化鐵膠體的方法為:向沸騰的蒸餾水中按適當比例滴加FeCl3飽和溶液,繼續加熱至液體呈紅褐色,停止加熱,故A正確;
B.稀釋濃硫酸時,應該將濃硫酸加入水中,順序不能顛倒,否則易導致酸液飛濺,故B錯誤;
C.濃氨水與生石灰反應制備干燥的NH3,由于硫酸與氨氣反應,應該用堿石灰干燥,故C錯誤;
D.乙酸乙酯和飽和碳酸鈉溶液分層后,應該先從分液漏斗下口放出飽和碳酸鈉溶液溶液,然后從分液漏斗的上口倒出有機層,故D錯誤;
故選A.
點評 本題考查了化學實驗方案的評價,題目難度不大,涉及氫氧化鐵膠體制備、氣體干燥、物質分離與提純、濃硫酸稀釋等知識,明確常見化學實驗基本操作方法為解答關鍵,試題有利于培養學生的化學實驗能力.


 字詞句篇與同步作文達標系列答案
字詞句篇與同步作文達標系列答案科目:高中化學 來源: 題型:選擇題
| A. | 飽和氯水中 Br-、NO3-、Na+、SO32- | |
| B. | 由水電離出的C(H+)=1×10 -12 mol•L-1的溶液:K+、Ba2+、HCO3-、Cl- | |
| C. | 0.1 mol•L-1FeCl3溶液:K+、NH4+、NO3-、SO42- | |
| D. | c(H+)/c(OH-)=1×10 -12的溶液:Ca2+、Fe3+、ClO-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
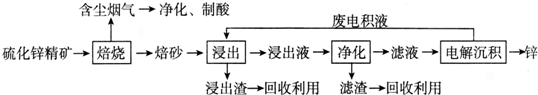
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2SO4(aq) | B. | HCl(aq) | C. | Fe2(SO4)3(aq) | D. | CuSO4(aq) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
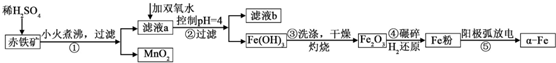
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | v(C)=v(D)=0.25mol•L-1•s-1 | B. | C的體積分數為28.6% | ||
| C. | B的轉化率為25% | D. | z=2 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
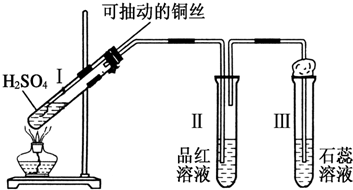
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com