
 最近報道了一種新型可充電式鋁電池.電解質為陽離子(EMl+)與陰離子(AlCl4-)組成的離子液體.如圖為該電池放電過程示意圖,Cn為石墨烯,下列說法不正確的是( )
最近報道了一種新型可充電式鋁電池.電解質為陽離子(EMl+)與陰離子(AlCl4-)組成的離子液體.如圖為該電池放電過程示意圖,Cn為石墨烯,下列說法不正確的是( )| A. | 充電時,每生成1mol Al,電解質溶液中會增加7molAlCl4- | |
| B. | 放電時,電解質中的陽離子(EMl+)未發生反應 | |
| C. | 放電時,負極反應方程式為Al+7AlCl4--3e-═4Al2Cl7- | |
| D. | 充電時,Cn為陽極,電極方程式為Cn+AlCl4--e-═Cn[AlCl4] |
分析 由示意圖可知放電時鋁為負極,被氧化生成Al2Cl7-,電極方程式為Al+7AlCl4--3e-═4Al2Cl7-,正極反應為3Cn[AlCl4]+3e-=3Cn+3AlCl4-,電解時陽極發生氧化反應,電解方程式為Cn+AlCl4--e-═Cn[AlCl4],陰極發生還原反應,電極方程式為4Al2Cl7-+3e-=Al+7AlCl4-,以此解答該題.
解答 解:A.充電時,陽極發生3Cn+3AlCl4--3e-═3Cn[AlCl4],陰極發生4Al2Cl7-+3e-=Al+7AlCl4-,每生成1mol Al,電解質溶液中會增加4molAlCl4-,故A錯誤;
B.放電時,負極Al+7AlCl4--3e-═4Al2Cl7-,正極發生3Cn[AlCl4]+3e-=3Cn+3AlCl4-,電解質中的陽離子(EMl+)未發生反應,故B正確;
C.由示意圖可知放電時鋁為負極,被氧化生成Al2Cl7-,電極方程式為Al+7AlCl4--3e-═4Al2Cl7-,故C正確;
D.充電時,Cn為陽極,發生氧化反應,電極方程式為Cn+AlCl4--e-═Cn[AlCl4],故D正確.
故選A.
點評 本題考查學生二次電池的工作原理以及原電池和電解池的工作原理知識,為高頻考點,側重學生的分析能力的考查,屬于綜合知識的考查,難度中等,注意把握電極的判斷方法和電極方程式的書寫.


科目:高中化學 來源: 題型:解答題
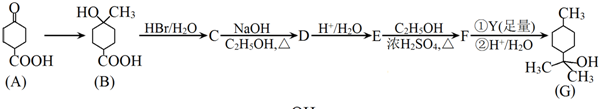
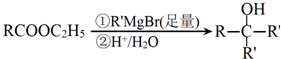
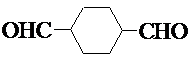 .
.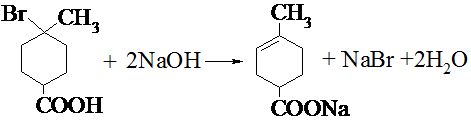 .
.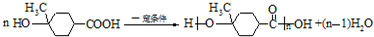 .
.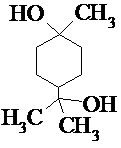 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溶液中的OH-向正極移動 | |
| B. | 在銀表面上的反應為:2Al+3Ag2S═6Ag+Al2S3 | |
| C. | 正極反應式為:Ag2S+2e-═2Ag+S2- | |
| D. | 在鋁表面的反應為:Al+3OH--3e-═Al(OH)3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
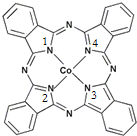 鈷(Co)是人體必需的微量元素.含鈷化合物作為顏料,具有悠久的歷史,在機械制造、磁性材料等領域也具有廣泛的應用.請回答下列問題:
鈷(Co)是人體必需的微量元素.含鈷化合物作為顏料,具有悠久的歷史,在機械制造、磁性材料等領域也具有廣泛的應用.請回答下列問題: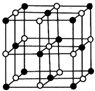 ,在該晶體中與一個鈷原子等距離且最近的鈷原子有12個;筑波材料科學國家實驗室一個科研小組發現了在 5K 下呈現超導性的晶體,該晶體具有CoO2的層狀結構(如下圖所示,小球表示Co原子,大球表示O原子).下列用粗線畫出的重復結構單元示意圖不能描述CoO2的化學組成的是D.
,在該晶體中與一個鈷原子等距離且最近的鈷原子有12個;筑波材料科學國家實驗室一個科研小組發現了在 5K 下呈現超導性的晶體,該晶體具有CoO2的層狀結構(如下圖所示,小球表示Co原子,大球表示O原子).下列用粗線畫出的重復結構單元示意圖不能描述CoO2的化學組成的是D.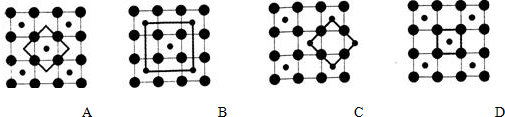
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
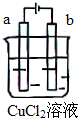
| A. | 電極a表面呈紅色 | |
| B. | 電極b表面有氣泡生成 | |
| C. | 電子由電源的負極沿導線流向電極b | |
| D. | 該裝置能量轉化形式為化學能轉化為電能 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.4mol/L | B. | 0.2mol/L | C. | 0.1mol/L | D. | 0.08mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 容器 | 甲 | 乙 |
| 反應物投入量 | 1mol CO2、3mol H2 | a mol CO2、b mol H2 c mol CH3OH(g)、c mol H2O(g) |
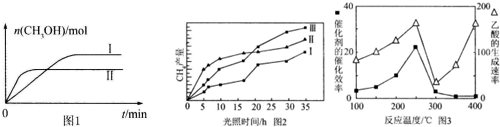
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com