
| A. | NH4Cl(s)═NH3(g)+HCl(g)室溫下不能自發進行,說明該反應的△H<0 | |
| B. | 鍍鋅鐵制品鍍層破損后,鐵制品比受損前更容易生銹,而鍍錫鐵則相反 | |
| C. | 對于N2(g)+3H2(g)?2NH3(g),當其他條件不變時,壓縮氣體體積使壓強增大,正反應和逆反應速率以及H2的平衡轉化率均增大 | |
| D. | 25℃時NH3•H2O稀溶液中,加水稀釋$\frac{c({H}^{+})•c(N{H}_{3}•{H}_{2}O)}{c(N{H}_{4}^{+})}$的值增大 |
分析 A.由反應可知△S>0,室溫下不能自發進行,則△H-T△S>0;
B.鍍鋅鐵制品鍍層破損后,構成原電池時Zn失去電子,鍍錫鐵鍍層破損后,構成原電池時Fe失去電子;
C.壓縮氣體體積使壓強增大,正逆反應速率均增大,平衡正向移動;
D.$\frac{c({H}^{+})•c(N{H}_{3}•{H}_{2}O)}{c(N{H}_{4}^{+})}$=Kh,只與溫度有關.
解答 解:A.由反應可知△S>0,室溫下不能自發進行,則△H-T△S>0,可知該反應的△H>0,故A錯誤;
B.鍍鋅鐵制品鍍層破損后,構成原電池時Zn失去電子,鐵制品比不易生銹;鍍錫鐵鍍層破損后,構成原電池時Fe失去電子,鐵制品比受損前更容易生銹,故B錯誤;
C.壓縮氣體體積使壓強增大,正逆反應速率均增大,平衡正向移動,則H2的平衡轉化率增大,故C正確;
D.$\frac{c({H}^{+})•c(N{H}_{3}•{H}_{2}O)}{c(N{H}_{4}^{+})}$=Kh,只與溫度有關,則25℃時NH3•H2O稀溶液中,加水稀釋$\frac{c({H}^{+})•c(N{H}_{3}•{H}_{2}O)}{c(N{H}_{4}^{+})}$的值不變,故D錯誤;
故選C.
點評 本題考查反應熱與焓變、原電池應用、平衡移動原理應用,為高頻考點,把握反應進行方向、電化學腐蝕、平衡移動為解答的關鍵,側重分析與應用能力的考查,注意化學反應原理的綜合應用,題目難度不大.


 學業測評一課一測系列答案
學業測評一課一測系列答案科目:高中化學 來源: 題型:解答題

| 編號 | 1 | 2 | 3 | 4 |
| 溶液的體積/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2標準溶液的體積/mL | 19.99 | 19.98 | 17.13 | 20.03 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 合成氨反應需使用催化劑,說明催化劑可以促進該平衡向生成氨的方向移動 | |
| B. | 常溫下,用蒸餾水不斷稀釋醋酸,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$的值變小 | |
| C. | 反應SiO2(s)+3C(s)=SiC(s)+2CO(g)室溫下不能自發進行,則該反應的△H<0 | |
| D. | 對于Ca(OH)2的沉淀溶解平衡,升高溫度,Ca(OH)2的溶解速率增大,Ksp減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某學生欲用已知物質的量濃度的鹽酸來測定未知物質的量濃度的NaOH溶液時,選擇甲基橙作指示劑.請填寫下列空白:
某學生欲用已知物質的量濃度的鹽酸來測定未知物質的量濃度的NaOH溶液時,選擇甲基橙作指示劑.請填寫下列空白:| 滴定次數 | 待測NaOH溶液的體積/mL | 0.100 0mol/L鹽酸的體積/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液體積/mL | ||
| 第一次 | 25.00 | 0.10 | 26.11 | 26.01 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.32 | 26.31 | 25.99 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
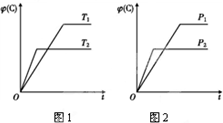 可逆反應m A(s)+n B(g)?e C(g)+f D(g),反應過程中,當其他條件不變時,C的體積分數φ(C)在不同溫度和不同壓強的條件下隨時間的變化如圖所示.下列敘述正確的是( )
可逆反應m A(s)+n B(g)?e C(g)+f D(g),反應過程中,當其他條件不變時,C的體積分數φ(C)在不同溫度和不同壓強的條件下隨時間的變化如圖所示.下列敘述正確的是( )| A. | 平衡后,若使用催化劑,C的體積分數將增大 | |
| B. | 平衡后,若溫度升高,化學平衡向正反應方向移動 | |
| C. | 平衡后,增加A的質量化學平衡向正反應方向移動 | |
| D. | 化學方程式中,化學計量數的關系為n<e+f |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
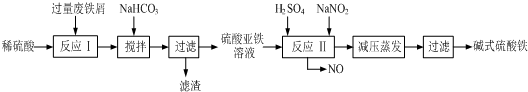
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 開始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 密閉容器中,9.6g 硫粉與 11.2g 鐵粉混合加熱生成硫化亞鐵 17.6g 時,放出 19.12KJ 熱量.則Fe(s)+S(s)═FeS(s)△H=-95.6KJ?mol-1 | |
| B. | 稀醋酸與 0.1mol?L-1NaOH 溶液反應:H+(aq)+OH-(aq)═H2O(l)△H=-57.3KJ?mol-1 | |
| C. | 已知,1molH2 完全燃燒生成液態水所放出的熱量為 285.5KJ,則水分解的熱化學方程式為:2H2O(l)═2H2(g)+O2(g)△H=-285.5KJ?mol-1 | |
| D. | 已知 2C(s)+O2(g)═2CO(g)△H=-221KJ?mol-1,則可知 C 的燃燒熱△H=-110.5KJ?mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 ;反應中1mol氧化劑得到 (填“得到”或“失去”)6mol電子.
;反應中1mol氧化劑得到 (填“得到”或“失去”)6mol電子.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com