
| 元素性質 編號 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半徑(10-10m) | 0.74 | 0.89 | 0.82 | 0.77 | 0.99 | 0.75 | 1.17 | 1.43 |
| 最高或最低化合價 | +2 | +3 | +4 | +7 | +5 | +4 | +3 | |
| -2 | -4 | -1 | -3 | -4 |

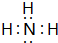 ;該物質溶于水后的溶液呈堿性(填“酸”、“堿”或“中”);
;該物質溶于水后的溶液呈堿性(填“酸”、“堿”或“中”);分析 ①沒有最高價、只有最低價-2,可推知①為O;③⑧都有最高價+3,處于ⅢA族,原子半徑③<⑧,故③為B、⑧為Al;④⑦都有最高價+4、最低價-4,處于ⅤA族,且④的原子半徑較小,故④為C、⑦為Si;⑤有最高價+7、最低價-1,則⑤為Cl;②只有有最高價+2,處于ⅡA族,原子半徑小于Cl,故②為Be;⑥有最高價+5、最低價-3,處于ⅤA族,原子半徑小于Cl,故⑥為N,據此解答.
解答 解:①沒有最高價、只有最低價-2,可推知①為O;③⑧都有最高價+3,處于ⅢA族,原子半徑③<⑧,故③為B、⑧為Al;④⑦都有最高價+4、最低價-4,處于ⅤA族,且④的原子半徑較小,故④為C、⑦為Si;⑤有最高價+7、最低價-1,則⑤為Cl;②只有有最高價+2,處于ⅡA族,原子半徑小于Cl,故②為Be;⑥有最高價+5、最低價-3,處于ⅤA族,原子半徑小于Cl,故⑥為N.
(1)②的元素符號是Be;③的元素名稱是:硼;①為O元素,在元素周期表中的位置是:第二周期ⅥA族,⑧的離子為Al3+,離子結構示意圖: ,
,
故答案為:Be;硼;第二周期ⅥA族; ;
;
(2)⑤和⑥的最高價氧化物對應水化物分別為HClO4、HNO3、,酸性大小:HClO4>HNO3,故答案為:HClO4;HNO3;
(3)⑥和⑦的氫化物分別為NH3、SiH4,非金屬性N>Si,故氫化物的穩定性:NH3>SiH4;NH3的氫化物電子式為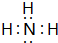 ;該物質溶于水后的溶液呈堿性,
;該物質溶于水后的溶液呈堿性,
故答案為:NH3;SiH4;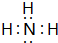 ;堿;
;堿;
(4)⑥的最高價氧化物對應水化物為HNO3、它的氫化物為NH3,二者反應的化學方程式:NH3+HNO3=NH4HNO3,故答案為:NH3+HNO3=NH4HNO3;
(5)⑧的最高價氧化物對應水化物為Al(OH)3,短周期中堿性最強的氫氧化物為NaOH,二者反應的離子方程式為:Al(OH)3+OH-=AlO2-+2H2O,
故答案為:Al(OH)3+OH-=AlO2-+2H2O;
(6)④的氫化物為CH4,與⑤的單質Cl2(體積比為1:2)在光照條件下反應,生成的有機產物有:一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷4種有機物,其中常溫下是氣體的是CH3Cl,含有4個相同極性鍵的是 CCl4,
故答案為:4;CH3Cl;CCl4.
點評 本題考查結構性質位置關系應用,難度中等,關鍵是根據化合價與原子半徑推斷元素,注意元素周期律的理解掌握.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
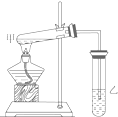 如圖是某學生設計的制取乙酸乙酯的實驗裝置圖,實驗中采取了以下主要實驗操作:
如圖是某學生設計的制取乙酸乙酯的實驗裝置圖,實驗中采取了以下主要實驗操作:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 C60、N60為新發現的有特殊用途的單質、分子結構均如圖所示.研究表明,C60、N60分子中所有均達到8電子穩定結構.
C60、N60為新發現的有特殊用途的單質、分子結構均如圖所示.研究表明,C60、N60分子中所有均達到8電子穩定結構.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 分子式 | 限定條件 | 數目 |
| A | C2H4O2 | 能與Na2CO3溶液反應 | 2 |
| B | C4H8Cl2 | 分子中有一個甲基 | 3 |
| C | C4H10O | 不能與鈉反應 | 2 |
| D | C8H10 | 含有苯環 | 3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
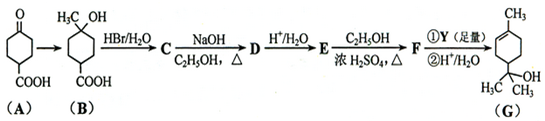
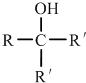
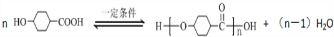
 .①核磁共振氫譜有2個吸收峰 ②能發生銀鏡反應
.①核磁共振氫譜有2個吸收峰 ②能發生銀鏡反應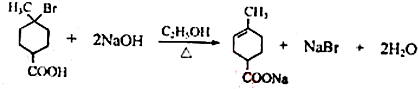 .
.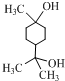 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com