
【題目】放熱反應2NO(g)+O2(g)![]() 2NO2(g)達平衡后,若分別采取下列一項措施:
2NO2(g)達平衡后,若分別采取下列一項措施:
①增大壓強 ②減小NO2的濃度 ③增大O2濃度 ④升高溫度 ⑤加入催化劑,能使平衡向正反應方向移動的是
A.①②③B.②③④C.③④⑤D.①②⑤
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化學 來源: 題型:
【題目】(題文)化合物N具有鎮痛、消炎等藥理作用,其合成路線如下:

(1)A的系統命名為____________,E中官能團的名稱為____________。
(2)A→B的反應類型為____________,從反應所得液態有機混合物中提純B的常用方法為____________。
(3)C→D的化學方程式為________________________。
(4)C的同分異構體W(不考慮手性異構)可發生銀鏡反應:且1 mol W最多與2 mol NaOH發生反應,產物之一可被氧化成二元醛。滿足上述條件的W有____________種,若W的核磁共振氫譜具有四組峰,則其結構簡式為____________。
(5)F與G的關系為(填序號)____________。
a.碳鏈異構 b.官能團異構 c.順反異構 d.位置異構
(6)M的結構簡式為____________。
(7)參照上述合成路線,以![]() 為原料,采用如下方法制備醫藥中間體
為原料,采用如下方法制備醫藥中間體![]() 。
。

該路線中試劑與條件1為____________,X的結構簡式為____________;
試劑與條件2為____________,Y的結構簡式為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將石油分餾得到的重油進行裂化可以獲得較多的輕質燃油。某研究性學習小組模擬工業.上石油的催化裂化設計了如圖所示實驗裝置。實驗過程中可觀察到燒瓶中固體石蠟先熔化,試管II中有少量液體生成,試管鞏中酸性高錳酸鉀溶液褪色,實驗后聞試管II中液體的氣味,發現其具有汽油的氣味。

資料一 石蠟是含有20 ~ 30個碳原子的烷烴組成的混合物,常溫下呈固態。
資料二 石油催化裂化過程中通常使用![]() 作催化劑。
作催化劑。
(1)為保證實驗成功,實驗前必須進行的操作是_________________;裝置中長導管的作用是________________________。
(2)試管II中有少量液體生成說明________________。
(3)試管III中溶液褪色說明_______________________。
(4)_______(填“能”或“不能”)用試管II中的液體萃取溴水中的溴,理由是___________。
(5)寫出二十烷裂化得到癸烷和癸烯的化學方程式:___________________________。
(6)石油裂化的主要目的是_______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E為元素周期表中前四周期元素,原子序數依次增大,A元素原子核外有3個未成對電子,B元素原子核外電子占用3個能級,其中最高能級上的電子數是其所在能層數的2倍,D元素與B元素同族,C元素與A元素同族,E元素原子的價電子數是其余電子數的一半。
(1)A、C、D的第一電離能由大到小的順序為___________________(用元素符號表示),E2+的基態電子排布式為__________________________________。
(2)B和D的氫化物中,B的氫化物沸點較高的原因是____________________________。
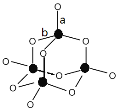
(3)C形成的最高價氧化物的結構如圖所示,該結構中C-B鍵的鍵長有兩類,鍵長較短的鍵為__________(填“a”或“b”)。
(4)E可與CO形成羰基配合物E2(CO)8,是有機合成的重要催化劑,不溶于水,溶于乙醇、乙醚、苯,熔點50~51℃,45℃(1.33kPa)時升華。
① E2(CO)8為_________晶體。(填晶體類型)
② E2(CO)8晶體中存在的作用力有______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CuCl為白色粉末,微溶于水,不溶于乙醇,潮濕的CuCl在空氣中被氧化為Cu2(OH)3Cl。
(1)一種由海綿銅(Cu)為原料制備CuCl的工藝流程如下:

①“溶解”步驟發生反應的離子方程式為_________________________________;
②潮濕的CuCl在空氣中被氧化的化學反應方程式為_________________________________;
③已知常溫下Cu(OH)2溶度積常數Ksp=2×10-20要使c(Cu2+)=0.2 mol·L-1的硫酸銅溶液中的銅離子沉淀比較完全(使銅離子濃度變為原來的千分之一)則應調節溶液pH為___________以上。
(2)次磷酸(H3PO2)是一元中強酸,可用于作金屬表面處理劑。
①向Ba(H2PO2)2溶液中加入硫酸可以制取H3PO2,寫出反應的化學方程式:_____________;
②H3PO2可將溶液中的Ag+還原為銀,從而用于化學鍍銀,反應同時生成P元素最高價氧化物對應的水化物。在該過程中,氧化劑與還原劑的物質的量之比為:___________;
③NaH2PO2的水溶液呈弱堿性,用離子方程式說明原因:______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作正確的是

A.實驗室保存飽和FeCl2溶液時,應加入少量鐵粉
B.將4.0gNaOH固體置于100mL容量瓶中,加水至刻度,配制1.000 mol·L-1 NaOH標準溶液,滴定未知濃度的鹽酸
C.用裝置甲蒸干AlCl3溶液制無水AlCl3固體
D.用裝置乙除去實驗室所制乙烯中的少量SO2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗不能達到預期實驗目的是()
序號 | 實驗內容 | 實驗目的 |
A | 室溫下,用pH試紙測定濃度為0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比較HClO和CH3COOH的酸性強弱 |
B | 向盛有1mL硝酸銀溶液的試管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 說明一種沉淀能轉化為另一種溶解度更小的沉淀 |
C | 向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,攪拌一會過濾 | 除去MgCl2中少量FeCl3 |
D | 室溫下,分別向2支試管中加入相同體積、相同濃度的Na2S2O3溶液,再分別加入相同體積不同濃度的稀硫酸 | 研究濃度對反應速率的影響 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表為元素周期表前4周期的一部分,下列有關R、W、X、Y、Z五種元素的敘述中,正確的是 ( )

A.W、R元素單質分子內都存在非極性鍵
B.X、Z元素都能形成雙原子分子
C.鍵長W—H<Y—H,鍵的極性Y—H>W—H
D.鍵長X—H<W—H,鍵能X—H<W—H
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖為元素周期表前四周期的一部分,下列有關R、W、X、Y、Z五種元素的敘述中,正確的是( )
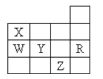
A.常壓下五種元素的單質中Z單質的沸點最高
B.Y、Z的陰離子電子層結構都與R原子的相同
C.W的氫化物的穩定性比X的氫化物的穩定性強
D.Y元素的非金屬性比W元素的非金屬性強
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com