
【題目】CuCl為白色粉末,微溶于水,不溶于乙醇,潮濕的CuCl在空氣中被氧化為Cu2(OH)3Cl。
(1)一種由海綿銅(Cu)為原料制備CuCl的工藝流程如下:

①“溶解”步驟發生反應的離子方程式為_________________________________;
②潮濕的CuCl在空氣中被氧化的化學反應方程式為_________________________________;
③已知常溫下Cu(OH)2溶度積常數Ksp=2×10-20要使c(Cu2+)=0.2 mol·L-1的硫酸銅溶液中的銅離子沉淀比較完全(使銅離子濃度變為原來的千分之一)則應調節溶液pH為___________以上。
(2)次磷酸(H3PO2)是一元中強酸,可用于作金屬表面處理劑。
①向Ba(H2PO2)2溶液中加入硫酸可以制取H3PO2,寫出反應的化學方程式:_____________;
②H3PO2可將溶液中的Ag+還原為銀,從而用于化學鍍銀,反應同時生成P元素最高價氧化物對應的水化物。在該過程中,氧化劑與還原劑的物質的量之比為:___________;
③NaH2PO2的水溶液呈弱堿性,用離子方程式說明原因:______________________。
【答案】3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O 4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl 6 Ba(H2PO2)2+H2SO4=2H3PO2+BaSO4↓ 4:1 H2PO2- + H2O![]() H2PO2- + OH-
H2PO2- + OH-
【解析】
(1)①“溶解”時NO3-在酸性條件下有氧化性,能溶解銅,相當于銅與稀硝酸的反應;
②結合題中所給出的反應物、生成物書寫相關方程式;
③利用Cu(OH)2溶度積常數,通過計算調節pH,使銅離子濃度變為原來的千分之一;
(2)①根據強酸制弱酸原理,向Ba(H2PO2)2溶液中加入硫酸可以制取H3PO2,同時生成BaSO4沉淀,則發生反應的化學方程式:Ba(H2PO2)2+H2SO4=2H3PO2+BaSO4↓;
②根據氧化還原反應中得失電子守恒,判斷出氧化劑與還原劑的物質的量之比;
③NaH2PO2是強堿弱酸鹽,H2PO2- 在溶液中水解使溶液呈堿性。
(1)①“溶解”時NO3-在酸性條件下有氧化性,能溶解銅,發生反應的離子方程式:3Cu+2 NO3-+8H+=3Cu2++2NO↑+4H2O ;
②潮濕的CuCl在空氣中被氧化Cu2(OH)3Cl的化學反應方程式:4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl;
③要使c(Cu2+)=0.2 mol·L-1的硫酸銅溶液中的銅離子沉淀比較完全(使銅離子濃度變為原來的千分之一),Ksp(Cu(OH)2)=0.2![]() 10-3
10-3![]() c2(OH-)=2×10-20,c(OH-)=1.0×10-8mol·L-1,pH=6,故應調節溶液pH為6以上;
c2(OH-)=2×10-20,c(OH-)=1.0×10-8mol·L-1,pH=6,故應調節溶液pH為6以上;
(2)①根據強酸制弱酸原理,向Ba(H2PO2)2溶液中加入硫酸可以制取H3PO2,同時生成BaSO4沉淀,則發生反應的化學方程式:Ba(H2PO2)2+H2SO4=2H3PO2+BaSO4↓;
②H3PO2可將溶液中的Ag+還原為銀,從而用于化學鍍銀,反應同時生成P元素最高價氧化物對應的水化物,應為H3PO4,H3PO2作還原劑,H3PO2→H3PO4,P元素的化合價從+1→+5,升高4價;Ag+作氧化劑Ag+→Ag,Ag元素的化合價從+1→0,降低1價,氧化還原反應中得失電子守恒,4、1的最小公倍數是4,氧化劑與還原劑的物質的量之比為4:1;
③NaH2PO2是強堿弱酸鹽,H2PO2- 在溶液中水解使溶液呈堿性,水解的離子方程式:H2PO2- + H2O![]() H2PO2- + OH-。
H2PO2- + OH-。


科目:高中化學 來源: 題型:
【題目】已知 A、B、C、D、E 都是周期表中前四周期的元素,且原子序數依次增大,其中 A 原子核外 有三個未成對電子;A 與 B 可形成離子化合物 B3A2;C 元素是地殼中含量最高的金屬元素;D 原 子核外的 M 層中有兩對成對電子;E 原子核外最外層只有 1 個電子,其余各層電子均充滿。以下 有關說法正確的是
A.A 離子半徑小于 B 離子半徑
B.B 和 C 的氯化物晶體類型相同
C.C 和 D 形成的二元化合物不能通過復分解反應得到
D.E 在周期表中位于第四周期 s 區
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對金屬制品進行腐蝕處理,可延長其使用壽命。
(1)以下為鋁材表面處理的一種方法:

①堿洗的目的是除去鋁材表面的自然氧化膜,堿洗時常有氣泡冒出,原因是__________________(用離子方程式表示)。
為將堿洗后槽液中的鋁以沉淀形式回收,最好向槽液中加入下列試劑中的__________。
a.NH3 b.CO2 c.NaOH d.HNO3
②以鋁材為陽極,在H2SO4溶液中電解,鋁材表面形成氧化膜,陽極的電極反應式為________________________________________________________________。
(2)鍍銅可防止鐵制品腐蝕,電鍍時用銅而不用石墨作陽極的原因是______________________________________________________________。
(3)利用如圖裝置,可以模擬鐵的電化學防護。
若X為碳棒,為減緩鐵的腐蝕,開關K應置于______處。
若X為鋅,開關K置于M處,該電化學防護法稱為_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】減少NO2、SO2、CO等有害氣體對大氣環境的危害,是人類的共同追求。
(1)在原子經濟學原則引導下,化學家用CO與H2在加熱加壓條件合成了液體燃料甲醇,其化學反應方程式___。
(2)以甲醇做燃料的電池,如圖所示,其負極是___(填a或b),負極的反應式為___,正極的反應式為___。該燃料電池在理想狀態下,將有96.5%的化學能轉化成電能,即消耗1mol液體甲醇所能產生的最大電能達702.1kJ,則通常甲醇燃燒的熱化學反應方程式為___。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業甲醇的質量分數可以用下列方法測定:
①在稀H2SO4中甲醇被Cr2O72-氧化成CO2和H2O,反應式為:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O;
②過量的Cr2O72-可用Fe2+與之完全反應:___Cr2O72-+__Fe2++__H+—__Cr3++__Fe3++__H2O。現有0.12g工業甲醇,在H2SO4溶液中與25mL0.2mol·L-1K2Cr2O7溶液反應,多余的K2Cr2O7再用1mol·L-1FeSO4與其反應,結果用去FeSO4溶液9.6mL。
(1)配平第②步的離子方程式___。
(2)計算工業甲醇的質量分數___。
(3)工業上通常利用SiO2和碳反應來制取硅,寫出反應的化學方程式__。
工業上還可以利用鎂制取硅,反應為2Mg+SiO2=2MgO+Si,同時會發生副反應:2Mg+Si=Mg2Si。如圖是進行Mg與SiO2反應的實驗裝置,試回答下列問題:
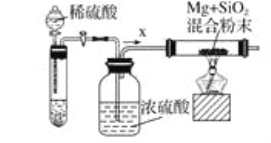
(4)由于O2和H2O(g)的存在對該實驗有較大影響,實驗中應通入氣體X作為保護氣,試管中的固體藥品可選用__(填序號)。
A.石灰石 B.鋅粒 C.純堿
(5)實驗開始時,必須先通一段時間X氣體,再加熱反應物,其理由是__;當反應引發后,移走酒精燈,反應能繼續進行,其原因是__。
(6)反應結束后,待冷卻至常溫時,往反應后的混合物中加入稀鹽酸,可觀察到閃亮的火星,產生此現象的原因是副產物Mg2Si遇鹽酸迅速反應生成SiH4(硅烷)氣體,然后SiH4自燃。用化學方程式表示這兩個反應①___,②___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素周期表的形式多種多樣,下圖是扇形元素周期表的一部分,對照中學化學常見長式元素周期表,回答下列問題:
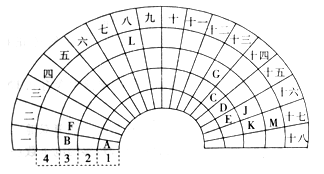
(1)元素C的最高價氧化物的電子式為____;元素G的離子結構示意圖為____。
(2)元素L位于周期表的第_________族,1mol/L LM2溶液500mL與0.4 mol K單質恰好完全反應的離子方程式為_______________________________________。
(3)化合物X是由B、E、G三種元素組成,其水溶液呈_____性,原因是____________(用離子方程式表示)。
(4)D和G組成的化合物GD,被大量用于制造電子元件。工業上用G的氧化物、C單質和D單質在高溫下制備GD,其中G的氧化物和C單質的物質的量之比為1:3,則該反應的化學方程式為___________。
(5)制取粗硅的過程中,SiO是反應中間產物,隔絕空氣時SiO和NaOH溶液反應(產物之一是硅酸鈉)的化學方程式______________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“碳捕捉技術”是指通過一定的方法將工業生產中產生的CO2分離出來并利用。如可利用NaOH溶液來“捕捉”CO2,其基本過程如圖所示(部分條件及物質未標出)。
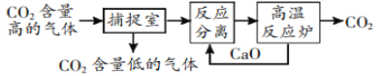
下列有關該方法的敘述中正確的是( )
①能耗大是該方法的一大缺點
②整個過程中,只有一種物質可以循環利用
③“反應分離”環節中,分離物質的基本操作是蒸發結晶、過濾
④該方法可減少碳排放,捕捉到的CO2還可用來制備甲醇等產品
A.①④B.②③C.③④D.①②
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸亞鐵銨[(NH4)2Fe(SO4)2]是分析化學中的重要試劑,在不同溫度下加熱分解產物不同。設計如圖實驗裝置(夾持裝置略去),在500℃時隔絕空氣加熱A中的硫酸亞鐵銨至分解完全。確定分解產物的成分。
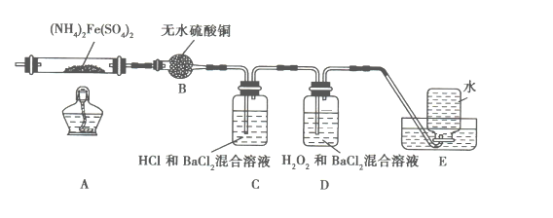
(1)B裝置的作用是_________。
(2)實驗中,觀察到C中無明顯現象,D中有白色沉淀生成,可確定產物中一定有_______氣體產生,寫出D中發生反應的離子方程式________。
(3)A中固體分解后產生NH3,寫出其兩種用途_________。
(4)用實驗的方法驗證C溶液含有NH4+:_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳有多種同素異形體,其中石墨烯與金剛石的晶體結構如圖所示,下列說法錯誤的是( )
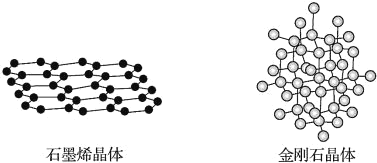
A.在石墨烯晶體中,每個C原子連接3個六元環
B.石墨烯晶體中的化學鍵全部是碳碳單鍵
C.在金剛石晶體中,C原子采用sp3雜化
D.在金剛石晶體中,六元環中最多有4個C原子在同一平面
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com