
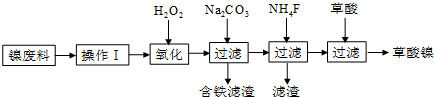
分析 流程分析,鎳廢料(鎳、鐵、鈣、鎂合金為主)制取草酸鎳(NiC2O4•2H2O),在高溫煅燒草酸鎳制取三氧化二鎳.鎳廢料加入酸溶解后過濾得到濾液中含有亞鐵離子、鈣離子、鎂離子、鎳離子,加入過氧化氫氧化亞鐵離子為鐵離子,加入碳酸鈉溶液調節溶液的PH,使鐵離子全部沉淀,過濾后的濾液在加入NH4F沉淀鈣離子和鎂離子,過濾得到溶液含有捏離子的溶液,在溶液中加入草酸生成草酸鎳,蒸發濃縮結晶析出晶體為目標產物NiC2O4•2H2O,
(1)鎳廢料中主要是鎳、鐵、鈣、鎂合金為主,操作Ⅰ是酸溶后過濾,溶解金屬,除去不溶物;
(2)過氧化氫氧化亞鐵離子為鐵離子,依據電荷守恒和原子守恒,加入Na2CO3溶液調pH至4.0〜4.5,促進鐵離子水解形成氫氧化鐵沉淀;
(3)草酸鎳(NiC2O4•2H2O)在熱空氣中干燥脫水后生成NiC2O4,NiC2O4再發生氧化還原反應(Ni由+2價升高到+3價,則C由+3價降低到+2價,題中要求生成混合氣體,則另一氣體為CO2)生成Ni2O3、CO、CO2,再利用化合價升降相等配平;
(4)Cl由+1價降低到-1價,Ni由+2價升高到+3價,利用化合價升降相等可配平ClO-、Ni(OH)2、Cl-、Ni2O3的系數,再利用H原子守恒配平水的系數,最后可利用O原子檢查配平是否正確;依據化學方程式和元素守恒計算得到;
(5)以Al和NiO(OH)為電極,NaOH溶液為電解液組成一種新型電池,放電時NiO(OH)轉化為Ni(OH)2,發生還原反應,則Al發生氧化反應,堿性條件下得到NaAlO2,配平書寫方程式.
解答 解:(1)分析框圖:“酸溶”生成含鎳、鐵、鈣、鎂離子的溶液,加酸溶解,溶解金屬,除去不溶物過濾;
故答案為:加酸溶解,過濾;
(2)①加雙氧水的目的是氧化生成Fe3+,反應的離子方程式為:2Fe2++H2O2+2H+═2Fe3++2H2O,
故答案為:2Fe2++H2O2+2H+═2Fe3++2H2O;
②加入碳酸鈉溶液的作用是調節pH,促進鐵離子水解沉淀完全,
故答案為:促進鐵離子水解沉淀完全;
(3)草酸鎳(NiC2O4•2H2O)在熱空氣中干燥脫水后生成NiC2O4,NiC2O4再發生氧化還原反應(Ni由+2價升高到+3價,則C由+3價降低到+2價,題中要求生成混合氣體,則另一氣體為CO2)生成Ni2O3、CO、CO2,再利用化合價升降相等,Ni:升高2×(3-2),C:升高1×(4-3),C:降低:3×(3-2),配平方程式為:2NiC2O4$\frac{\underline{\;高溫\;}}{\;}$Ni2O3+3CO↑+CO2↑;
故答案為:2NiC2O4$\frac{\underline{\;高溫\;}}{\;}$Ni2O3+3CO↑+CO2↑;
(4)Cl由+1價降低到-1價,Ni由+2價升高到+3價,利用化合價升降相等可配平ClO-、Ni(OH)2、Cl-、Ni2O3的系數,再利用H原子守恒配平水的系數,最后可利用O原子檢查配平是否正確,得到離子方程式為:ClO-+2Ni(OH)2═Cl-+Ni2O3+2H2O;
ClO-+2Ni(OH)2═Cl-+Ni2O3+2H2O
1 2
n(ClO-) a mol
則n(ClO-)=0.5 a mol
Cl2+2OH-═ClO-+Cl-+H2O
0.8n(Cl2) 0.5 a mol
則n(Cl2)=0.625 a mol
進行電解時:
2Cl--2e-═Cl2↑
2 1
n(e-) 0.625 a mol
則n(e-)=1.25a mol;
故答案:ClO-+2Ni(OH)2═Cl-+Ni2O3+2H2O;1.25a mol;
(5)以Al和NiO(OH)為電極,NaOH溶液為電解液組成一種新型電池,放電時NiO(OH)轉化為Ni(OH)2,發生還原反應,則Al發生氧化反應,堿性條件下得到NaAlO2,該電池反應的化學方程式是:Al+3NiO(OH)+NaOH+H2O=3Ni(OH)2+NaAlO2,
故答案為:Al+3NiO(OH)+NaOH+H2O=3Ni(OH)2+NaAlO2.
點評 本題考查了流程分析推斷,實驗操作步驟的分析判斷,化學方程式計算和電解原理分析應用,題目綜合性較大,難度較大.


 智趣寒假作業云南科技出版社系列答案
智趣寒假作業云南科技出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | 20:1 | B. | 1:20 | C. | 10:1 | D. | 1:10 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| 選項 | 現象 | 結論 |
| A | ①中導管口冒氣泡,手松開無現象 | 氣密性良 |
| B | ②中KMnO4溶液紫紅色褪去 | SO2具有漂白性 |
| C | ③中關閉K,氣體顏色在熱水中比冷水深 | NO2生成N2O4為吸熱反應 |
| D | ④中燒瓶中形成噴泉 | Cl2易溶于CCl4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 在一定條件下,根據溶液導電性的變化,可以判斷出電解質的強弱.已知溶液的導電性與溶液自由移動離子的濃度及其所帶電荷有關.離子濃度越大,所帶電荷越多,導電性就越強,如圖是將KOH溶液分別加入到相同物質的量濃度的HCl溶液和CH3COOH溶液中的導電性變化情況.下列說法正確的是( )
在一定條件下,根據溶液導電性的變化,可以判斷出電解質的強弱.已知溶液的導電性與溶液自由移動離子的濃度及其所帶電荷有關.離子濃度越大,所帶電荷越多,導電性就越強,如圖是將KOH溶液分別加入到相同物質的量濃度的HCl溶液和CH3COOH溶液中的導電性變化情況.下列說法正確的是( )| A. | 虛線表示CH3COOH溶液,實線表示HCl溶液 | |
| B. | 由圖可知,HCl溶液中加入KOH溶液后導電性將進一步增強 | |
| C. | 由圖可知,加入KOH溶液到一定量后,導電性均會比原來強 | |
| D. | 若用NH3•H2O溶液加入到HCl溶液中,則導電性變化如圖 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
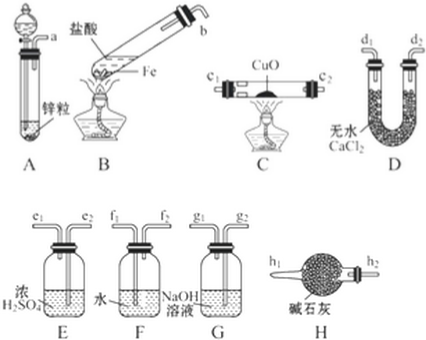
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 第2周期元素的第一電離能隨原子序數遞增依次增大 | |
| B. | 氟元素的電負性最大 | |
| C. | CO2、SO2都是直線形的非極性分子 | |
| D. | CH2═CH2分子中共有四個σ鍵和一個π鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 同溫同濃度Na2CO3和Na2SiO3水溶液的pH前者小于后者,則碳的非金屬性強于硅 | |
| B. | 向淀粉溶液中加入稀硫酸,加熱幾分鐘,冷卻后加新制Cu(OH)2懸濁液,加熱,無磚紅色沉淀,則淀粉沒有水解成葡萄糖 | |
| C. | 向無色溶液中加入氯水,再加CCl4,振蕩靜置后CCl4層呈紫色,則原溶液中含I- | |
| D. | 向某溶液中加入稀鹽酸,產生的氣體通入澄清石灰水,石灰水變渾濁,該溶液中一定含有CO32-或HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 混合物 | 試劑 | 分離方法 | |
| A | 苯(苯酚) | 溴水 | 過濾 |
| B | 甲烷(甲醛) | 水、濃硫酸 | 洗氣 |
| C | 乙酸乙酯(乙酸) | 氫氧化鈉溶液 | 蒸餾 |
| D | 淀粉膠體(氯化鈉溶液) | 蒸餾水 | 萃取 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com