
| A. | HCl═H++Cl- | B. | NH3•H2O═NH4++OH- | ||
| C. | CaCl2=Ca2++2Cl- | D. | CH3COOH?CH3COO-+H+ |
科目:高中化學 來源: 題型:選擇題
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 0~2 min的平均速率v(Z)=2.0×10-3 mol•L-1•min-1 | |
| B. | 其他條件不變,降低溫度,反應達到新平衡時v(正)>v(逆) | |
| C. | 該溫度下此反應的平衡常數K=144 | |
| D. | 其他條件不變,再充入0.2 mol Z,平衡時X的體積分數不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
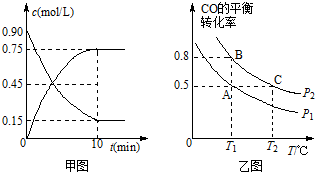
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Z>X>Y | B. | X>Y>Z | C. | Y>X>Z | D. | Y>Z>X |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NA個18O2和NA個NO的質量比為16:15 | |
| B. | 標準狀況下1molCO和CO2的混合物的體積約占22.4L | |
| C. | 24gMg在足量空氣中完全燃燒失去2NA個電子 | |
| D. | 常溫下,18gH2O含有的電子數為10NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 可用澄清石灰水鑒別Na2CO3和NaHCO3溶液 | |
| B. | 濃硫酸具有吸水性,可做干燥劑,但不能干燥NH3 | |
| C. | 鈉保存在煤油中,若長期放置在空氣中,最終變為NaHCO3 | |
| D. | 鎂著火后可以用CO2來滅火 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
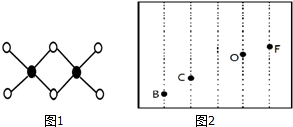 硼及其化合物在工業上有許多用途.工業上以鐵硼礦為原料制備硼酸,鐵硼礦含有Mg、Fe、Ca、Al、B、O等多種元素,它的主要成分為Mg2B2O5•H2O和Fe3O4.
硼及其化合物在工業上有許多用途.工業上以鐵硼礦為原料制備硼酸,鐵硼礦含有Mg、Fe、Ca、Al、B、O等多種元素,它的主要成分為Mg2B2O5•H2O和Fe3O4.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com